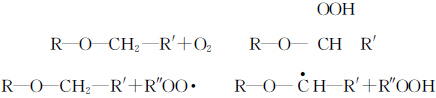Apa efek monomer UV pada pemblokiran oksigen yang dapat disembuhkan oleh UV?
1.2 Persiapan dan pengujian sampel
Monomer dan inisiator ditimbang secara akurat, di mana monomer tidak dimurnikan, dan dicampur secara seragam dengan pengaduk magnetik. UV-DSC digunakan untuk melakukan eksperimen pengawetan UV di bawah atmosfer udara statis dan atmosfer nitrogen, dan sampel diambil dalam jumlah yang sama setiap kali sehingga ketebalan sampel dalam wadah sama. Program UV-DSC diatur untuk menjaga suhu sampel konstan selama 2 menit, kemudian sumber cahaya secara otomatis dihidupkan oleh program, dan sinar UV (rentang panjang gelombang 325-400 nm) dimasukkan ke dalam sel DSC oleh serat kaca untuk menerangi wadah sampel dan wadah referensi, dan DSC mengukur nilai aliran panas dari proses pemotretan sampel. Intensitas cahaya diukur sebagai 48,27 mW-cm-2. Intensitas cahaya ditentukan dengan menyebarkan karbon hitam di bagian bawah wadah sampel, dan energi yang diserap oleh cahaya diukur dengan UV-DSC dan dibagi dengan area dasar wadah untuk mendapatkan intensitas cahaya.
2 Hasil dan pembahasan
2.1 Pemrosesan data
Laju curing ringan dihitung sebagai
Laju pengeringan cahaya R = dC/dt = (dH/dt) / Hmax, di mana dH/dt adalah nilai aliran panas pada kurva entalpi versus waktu proses pengeringan cahaya yang diukur dengan UV-DSC; Hmax adalah total panas polimerisasi sampel pada 200 detik paparan cahaya, yang diperoleh dengan mengintegrasikan puncak eksotermik pengeringan cahaya. Waktu yang sesuai dengan laju pengawetan maksimum dari proses pengawetan cahaya adalah tmax. Polimerisasi radikal bebas akan terjadi secara otomatis fenomena percepatan, kurva laju curing cahaya terhadap turunan waktu, nilai maksimum kurva yang sesuai dengan waktu yang dicatat sebagai tamax, waktu ini dapat dianggap sebagai waktu tercepat dari laju curing cahaya, pada saat ini sistem pemblokiran oksigen dan efek sangkar serta faktor lain pada konsumsi radikal primer seminimal mungkin. Monomer pemrakarsa radikal bebas mulai berpolimerisasi dengan cepat.
Perhitungan kandungan inisiator (fraksi molar) α dalam sampel:
Di mana n inisiator adalah jumlah molar inisiator dalam sistem, f adalah derajat fungsional monomer, dan n monomer adalah jumlah molar monomer dalam sistem. Gambar 1 menunjukkan struktur molekul inisiator Irgacure-184, yang merupakan tipe pembelahan, dan "2" dalam rumus (1) berarti bahwa satu molekul inisiator secara teoritis dapat diuraikan menjadi dua molekul radikal oleh paparan cahaya.
Formula struktural Irgacure-184
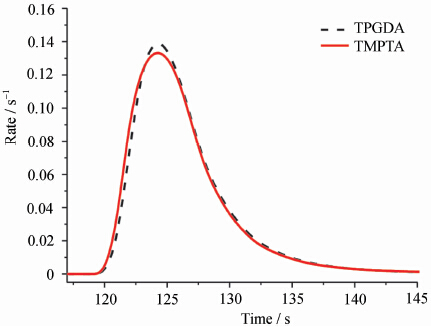
Gambar 2 menunjukkan kurva laju curing cahaya monomer yang berbeda pada kandungan inisiator 4% (fraksi massa). Seperti yang dapat dilihat dari gambar, untuk monomer yang berbeda, terdapat perbedaan laju curing pada periode pra-curing, dan perbedaan ini juga dinyatakan dalam waktu, yang mengindikasikan bahwa curing UV monomer yang berbeda dalam waktu yang berbeda pula dalam kecepatan. Waktu tamax ketika laju curing cahaya monomer tumbuh paling cepat dan waktu tmax yang sesuai dengan laju curing cahaya maksimum dibandingkan dengan kurva variasi konten inisiator, dan hasilnya ditunjukkan pada Gambar 3.
Kurva laju pengawetan UV dari monomer yang berbeda dengan inisiator 4%
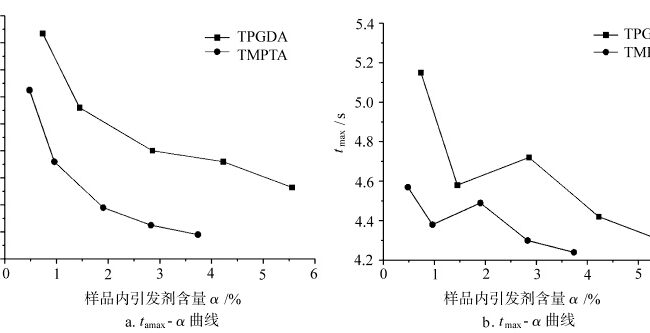
Hubungan dari tamax dan tmaks dengan kandungan inisiator dalam proses pengawetan di udara dengan monomer yang berbeda
Gambar 3 menunjukkan kurva tmax dan tamax untuk pengawetan cahaya monomer yang berbeda di bawah udara sebagai fungsi dari kandungan inisiator α dalam sampel. Pada tahap awal pengawetan, apabila terdapat oksigen, sebagian radikal reaktif yang dihasilkan oleh photoinisiator akibat cahaya dikonsumsi oleh oksigen yang dilarutkan dalam sampel, dan bagian lainnya memulai polimerisasi monomer. Efek pemblokiran oksigen mengonsumsi radikal yang dihasilkan oleh penguraian inisiator dan radikal monomer, sehingga memengaruhi besarnya tamax dan tmax curing cahaya, yang pada gilirannya merefleksikan sensitivitas curing cahaya terhadap kandungan oksigen dan inisiator. Seperti yang terlihat pada Gbr. 3a, tamax dari setiap monomer light curing menurun dengan meningkatnya kandungan inisiator dalam pola tertentu. Pada Gbr. 3b, tmax dari setiap light curing monomer menunjukkan fluktuasi tertentu dengan peningkatan kandungan inisiator. Hal ini karena ketika laju reaksi curing mencapai maksimum, sistem telah mencapai tingkat curing yang tinggi, dan segmen rantai molekul secara bertahap dibekukan karena efek kaca, dan sensitivitas tmax reaksi curing cahaya terhadap kandungan inisiator berkurang saat ini. Sementara tamax pada tahap awal curing ringan, ketika sistem tidak memiliki tingkat curing yang tinggi, reaksi curing ringan lebih sensitif terhadap kandungan inisiator dalam sistem. Oleh karena itu, sebagai perbandingan, tamax lebih mencerminkan sensitivitas light curing terhadap kandungan inisiator.
2.2 Pengaruh atmosfer pada tamax pengawetan cahaya dari monomer yang berbeda
Dalam atmosfer udara, tamax bahan yang difotokopi harus berbeda dibandingkan dengan atmosfer nitrogen karena efek pemblokiran oksigen. Pengujian UV-DSC dilakukan pada monomer TMPTA di bawah atmosfer udara dan nitrogen ketika kandungan inisiator yang lebih rendah ditambahkan, dan hasilnya tercantum dalam Tabel 1.
| tamaxtamax dari pengawetan UV TMPTA dengan kandungan inisiator rendah di udara atau N2 | ||
| Kandungan inisiator dalam sampel / % | tamax/s | |
| udara | N2 | |
| 0.48 | 2.65 | 2.18 |
| 0.96 | 2.12 | 1.92 |
tamax dari TMPTA UV-curing dengan kandungan inisiator rendah di udara atau N2
Tabel 1 menunjukkan perbandingan tamax TMPTA yang difoto di bawah udara dan nitrogen, masing-masing dengan penambahan inisiator yang lebih rendah. Dari tabel di atas, dapat dilihat bahwa tamax curing ringan di bawah udara lebih besar daripada di bawah nitrogen ketika kandungan inisiatornya sama, yang mengindikasikan bahwa curing ringan di bawah udara dipengaruhi oleh penghalangan oksigen. Secara umum diyakini bahwa oksigen yang terlarut dalam bahan baku serta di permukaan mengalami reaksi berikut selama proses curing ringan.
Radikal peroksida yang dihasilkan ROO- sangat stabil dan tidak memiliki kemampuan untuk memulai reaksi polimerisasi. Oksigen tidak hanya membersihkan radikal yang dihasilkan oleh inisiator selama proses pengawetan ringan, tetapi juga menghentikan radikal monomer.
Sensitivitas pemotretan terhadap polimerisasi penghambat oksigen bervariasi untuk monomer yang berbeda dan terkait dengan faktor-faktor seperti fungsi monomer, aktivitas ikatan rangkap, dan struktur [13]. Untuk menyelidiki pengaruh struktur monomer pada agregasi penghambat oksigen, dua TMPTA ber-EO yang berbeda dipilih untuk eksperimen UV-DSC dalam kondisi udara dan nitrogen. Semua monomer homolog ini memiliki struktur yang serupa, kecuali jumlah gugus EO, yang menghindari masalah yang rumit dengan memilih beberapa monomer lain dengan struktur yang sangat berbeda [13].
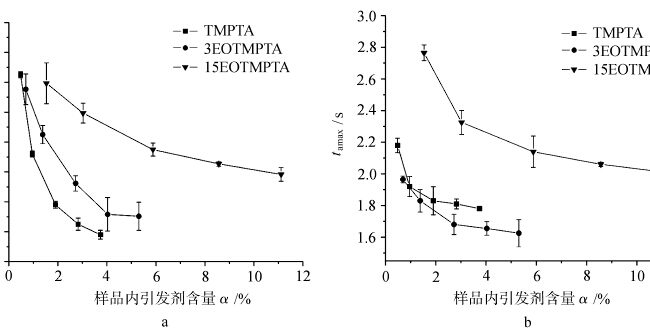
Gambar 4 menunjukkan variasi tamax dengan kandungan inisiator di dalam sampel untuk pengawetan ringan monomer TMPTA dengan EOisasi yang berbeda di bawah udara dan nitrogen. Seperti yang terlihat pada gambar, tamax dari setiap monomer yang difoto di bawah udara dan nitrogen menurun dengan bertambahnya kandungan inisiator. Variasi tamax yang diawetkan dengan cahaya dari setiap monomer di bawah udara dan nitrogen bervariasi dengan jumlah EO dalam monomer. Hal ini menunjukkan bahwa jumlah EO dalam monomer berpengaruh pada tamax light curing. Untuk monomer yang sama, perbedaan tamax curing ringan di bawah udara dan nitrogen terkait dengan penghalang oksigen ketika kondisi lainnya sama.
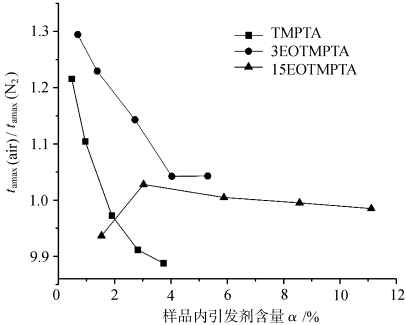
Gambar 5 menunjukkan kurva rasio tamax masing-masing monomer yang difotokopi di bawah atmosfer yang berbeda dengan variasi kandungan inisiator α. tamax (udara) / tamax (N2) menunjukkan perbedaan tamax monomer yang difotokopi di bawah udara dan nitrogen, sehingga merefleksikan besarnya penghalangan oksigen masing-masing monomer yang difotokopi, semakin besar nilainya, maka efek penghalangan oksigennya juga akan semakin besar. Seperti yang terlihat pada Gambar 5, rasio tamax (udara) / tamax (N2) dari monomer TMPTA dan monomer 3EOTMPTA lebih besar ketika konten inisiator kecil dan menurun dengan meningkatnya konten inisiator. Hal ini menunjukkan bahwa monomer TMPTA dan monomer 3EOTMPTA tunduk pada efek pemblokiran oksigen yang lebih signifikan ketika kandungan inisiatornya kecil. Ketika jumlah EO dalam monomer mencapai 15, rasio tamax (udara) / tamax (N2) dari monomer mendekati 1, yaitu, ada sedikit perbedaan dalam tamax curing ringan dalam kondisi udara atau nitrogen, yang menunjukkan bahwa peningkatan jumlah EO dalam monomer bermanfaat untuk mengurangi polimerisasi pemblokiran oksigen pada curing UV, yang mungkin terkait dengan hidrogen aktif dalam struktur EO. struktur seperti eter di bagian EO α-H pada -O-CH2- mudah disubstitusi oleh oksigen dan reaksi berikut terjadi.
Hubungan dari tamax(udara)/tamax(N2) dengan kandungan inisiator dalam proses pengawetan TMPTA teretoksilasi yang berbeda.
α-H di satu sisi dapat mengkonsumsi sebagian oksigen dalam sistem, di sisi lain, dapat menghentikan radikal peroksida ROO- yang dihasilkan oleh radikal dan oksigen, sehingga mengurangi konsumsi radikal reaktif dan mengarahkan aktivitas inisiasi ke segmen rantai dengan aktivitas inisiasi, sehingga mengurangi pemblokiran oksigen pada proses pengawetan cahaya.
2.3 Pengaruh jumlah α-H dalam monomer pada agregasi pemblokiran oksigen yang mengawetkan cahaya
Untuk menyelidiki hubungan antara pemblokiran oksigen dan jumlah α-H dalam gugus EO monomer, kurva tamax-α pada Gambar 4 dipasang secara linier ke persamaan yang berbeda, dan ditemukan bahwa koefisien korelasi tertinggi diperoleh dengan memasang secara linier persamaan lnt = a + b / α0,5. Kemiringan b yang diperoleh dari pencocokan dan koefisien korelasi R tercantum dalam Tabel 2.
| Nilai b dan R dengan kecocokan linier 1/α0,5 dan lnt | ||||
| Monomer | udara | N2 | ||
| b | R | b | R | |
| TMPTA | 0.056 | 0.99894 | 0.0213 | 0.95494 |
| EO3TMPTA | 0.0554 | 0.95877 | 0.0257 | 0.98564 |
| 15EOTMPTA | 0.0531 | 0.96578 | 0.062 | 0.98944 |
Membandingkan nilai μ yang sesuai dengan monomer yang berbeda pada Gambar 6, μ memiliki nilai maksimum ketika monomernya adalah TMPTA, yaitu, efek penghalang oksigen paling besar ketika monomer TMPTA diawetkan dengan sinar UV. Ketika jumlah EO dalam monomer meningkat, jumlah α-H dalam monomer meningkat dan nilai μ menurun, menunjukkan bahwa penghalang oksigen terkait dengan jumlah α-H dalam monomer, yang memerangkap oksigen dan radikal peroksida dalam sistem dan mengurangi penghalang oksigen. Viskositas merupakan sifat yang berkaitan dengan struktur molekul, yang melibatkan sifat aliran monomer, sehingga perlu dibahas lebih lanjut mengenai pengaruh sifat aliran monomer terhadap polimerisasi penghalang oksigen.
2.4 Pengaruh sifat aliran monomer pada agregasi penghalang oksigen
Sifat aliran sistem terkait dengan struktur molekul. Secara umum, semakin fleksibel rantai molekul, semakin rendah penghalang rotasi di dalam rantai, semakin pendek segmen rantai sebagai unit bergerak, dan semakin rendah energi aktivasi rantai molekul fleksibel, semakin baik mobilitasnya. Semakin besar berat molekul, semakin besar hambatan gesekan internal terhadap gerakan molekul dan mobilitas yang buruk [19]. Oleh karena itu, pengenalan gugus EO dalam monomer TMPTA akan mengubah sifat aliran sistem. Menggunakan rheometer dengan laju geser konstan 19,1 / menit dan laju kenaikan suhu 2 ° C / menit, kurva viskositas masing-masing monomer diukur dengan suhu. Kurva viskositas-suhu dari masing-masing monomer disesuaikan dengan persamaan Arrhenius, dan energi aktivasi aliran yang dihitung E, prefaktor A, dan viskositas monomer η pada suhu 25 °C dicantumkan dalam Tabel 3.
| Nilai viskositas η (25 ℃), energi aktivasi aliran E, dan faktor pra-eksponensial A dari monomer | |||
| Monomer | η/Pa-s (25 ℃) | A/10-8 | E/J |
| TMPTA | 0.01934 | 15.53 | 29079.88 |
| 3EOTMPTA | 0.06948 | 2.65 | 36600.47 |
| 15EOTMPTA | 0.18016 | 6.28 | 36821.87 |
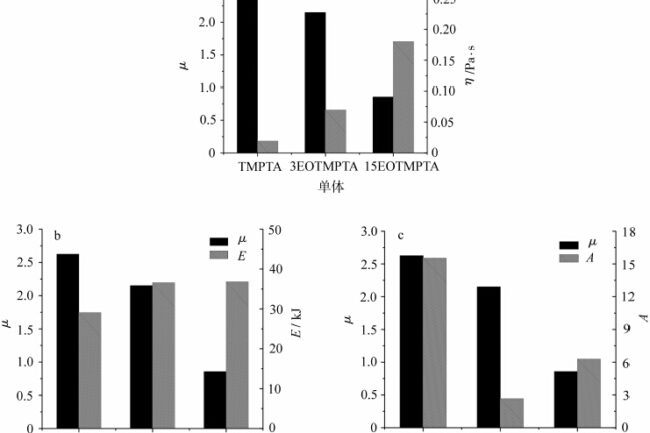
Di antaranya, energi aktivasi aliran E terkait dengan struktur molekul dan dipengaruhi oleh kekakuan dan fleksibilitas rantai molekul, ukuran dan polaritas gugus samping, dll. Faktor depan indeks A adalah konstanta yang terkait dengan berat molekul. Untuk menyelidiki hubungan antara sifat aliran monomer dan penghalang oksigen, nilai μ dari monomer yang berbeda dikorelasikan dengan viskositas yang sesuai η, energi aktivasi aliran E dan faktor awal A, seperti yang ditunjukkan pada Gambar 7.
Gambar 7 menunjukkan perbandingan nilai μ dari monomer yang berbeda dalam kaitannya dengan energi aktivasi aliran E, faktor depan jari A, dan viskositas η. Seperti yang terlihat pada Gbr. 7a, nilai μ cenderung menurun seiring bertambahnya jumlah EO dalam monomer dan meningkatnya viskositas monomer. Ukuran agregasi pemblokiran oksigen berkaitan erat dengan konsentrasi oksigen, dan semakin besar konsentrasi oksigen, semakin jelas pemblokiran oksigen [7]. Di bagian dalam sistem pengawetan cahaya, jumlah oksigen terlarut sudah pasti, dan laju pendinginan dan pemulungan radikal bebas oleh oksigen dalam proses pengawetan cahaya sangat cepat, dan oksigen yang dikonsumsi sebagian besar diisi ulang oleh difusi oksigen dari udara ke bagian dalam sistem secara terus menerus, yang tentunya akan melibatkan kemampuan pergerakan oksigen dalam sistem, dan kemampuan pergerakan oksigen dalam sistem terkait dengan viskositas sistem. Ketika viskositas sistem rendah, oksigen di udara lebih mudah berdifusi ke bagian dalam sistem, menunjukkan efek pemblokiran oksigen yang lebih besar, sehingga nilai μ monomer TMPTA lebih tinggi dan secara signifikan terhalang oleh oksigen. Ketika viskositas sistem meningkat, kemampuan pergerakan oksigen dalam sistem menurun dan sudah terlambat untuk mengisi kembali oksigen yang dikonsumsi dengan membersihkan radikal bebas, dan pemblokiran oksigen menurun. Seperti yang dapat dilihat dari gambar, ketika jumlah EO dalam monomer meningkat menjadi 15, viskositas monomer terus meningkat dan nilai μ cenderung ke 1, yaitu, perbedaan antara pengawetan ringan di bawah udara dan nitrogen tidak signifikan.
Kemudian bandingkan energi aktivasi aliran dan faktor depan jari-jari monomer dengan nilai μ. Seperti yang terlihat pada Gambar 7b, energi aktivasi aliran monomer meningkat dari TMPTA ke 3EOTMPTA dengan diperkenalkannya gugus EO dalam monomer. Ketika jumlah EO dalam monomer ditingkatkan dari 3 menjadi 15, energi aktivasi aliran pada dasarnya tidak berubah, yang menunjukkan bahwa peningkatan jumlah EO dalam monomer pada dasarnya tidak berpengaruh pada energi aktivasi aliran. Hal ini karena meskipun jumlah EO dalam monomer meningkat, jumlah unit kinematik tidak berubah, yang menunjukkan bahwa untuk monomer TMPTA ber-EO, efek energi aktivasi aliran pada penghalang oksigen tidak signifikan. Seperti yang terlihat pada Gbr. 7c, prefaktor jari A sangat berubah dari TMPTA menjadi 3EOTMPTA, yang mungkin terkait dengan ada atau tidak adanya gugus EO. Dengan bertambahnya jumlah EO dalam monomer, prefaktor A meningkat, yang disebabkan oleh peningkatan jumlah EO dalam monomer yang menyebabkan peningkatan berat molekul monomer. Dapat ditunjukkan bahwa untuk monomer TMPTA ber-EO, peningkatan jumlah EO dalam molekul menyebabkan peningkatan berat molekul, yang menyebabkan peningkatan viskositas monomer dan dengan demikian mengurangi penghalang oksigen. Untuk bahan polimer, viskositas sistem secara umum dapat ditingkatkan dengan meningkatkan kekakuan rantai molekul, meningkatkan polaritas gugus samping, meningkatkan berat molekul, dll.. Dapat diduga bahwa efek buruk dari pemblokiran oksigen pengawet cahaya dapat dikurangi dengan komposisi formulasi yang sesuai, seperti memasukkan struktur yang mengandung hidrogen aktif, meningkatkan proporsi molekul kaku, dan meningkatkan berat molekul.
3 Kesimpulan
(1) Meningkatkan jumlah gugus EO dalam molekul monomer dapat mengurangi agregasi penghalang oksigen selama proses pengawetan ringan. Hal ini terkait dengan terperangkapnya oksigen dan radikal peroksida oleh α-H dalam kelompok ini dan peningkatan viskositas sistem.
(2) Untuk beberapa TMPTA ber-EO yang dipilih untuk penelitian ini, energi aktivasi aliran monomer memiliki efek yang kecil pada agregasi penghalang oksigen. Peningkatan jumlah EO dalam monomer menyebabkan peningkatan berat molekulnya, yang menyebabkan peningkatan viskositas monomer, yang pada gilirannya berpengaruh pada agregasi penghalang oksigen.
Monomer UV Produk seri yang sama
| Polythiol / Polymercaptan | ||
| Monomer DMES | Bis (2-merkaptoetil) sulfida | 3570-55-6 |
| Monomer DMPT | THIOCURE DMPT | 131538-00-6 |
| Monomer PETMP | 7575-23-7 | |
| PM839 Monomer | Polioksi (metil-1,2-etanadiil) | 72244-98-5 |
| Monomer Monofungsional | ||
| Monomer HEMA | 2-hidroksietil metakrilat | 868-77-9 |
| Monomer HPMA | 2-Hidroksipropil metakrilat | 27813-02-1 |
| Monomer THFA | Tetrahidrofurfuril akrilat | 2399-48-6 |
| Monomer HDCPA | Diklopentenil akrilat terhidrogenasi | 79637-74-4 |
| Monomer DCPMA | Dihydrodicyclopentadienyl methacrylate | 30798-39-1 |
| Monomer DCPA | Dihydrodicyclopentadienyl Acrylate | 12542-30-2 |
| Monomer DCPEMA | Dicyclopentenyloxyethyl Methacrylate | 68586-19-6 |
| Monomer DCPEOA | Dicyclopentenyloxyethyl Acrylate | 65983-31-5 |
| Monomer NP-4EA | (4) nonilfenol teretoksilasi | 50974-47-5 |
| LA Monomer | Lauril akrilat / Dodesil akrilat | 2156-97-0 |
| Monomer THFMA | Metakrilat tetrahidrofurfuril | 2455-24-5 |
| Monomer PHEA | 2-FENOKSIETIL AKRILAT | 48145-04-6 |
| Monomer LMA | Lauril metakrilat | 142-90-5 |
| IDA Monomer | Isodecyl acrylate | 1330-61-6 |
| IBOMA Monomer | Isobornil metakrilat | 7534-94-3 |
| IBOA Monomer | Isobornil akrilat | 5888-33-5 |
| Monomer EOEOEA | 2- (2-Etoksietoksi) etil akrilat | 7328-17-8 |
| Monomer multifungsi | ||
| Monomer DPHA | 29570-58-9 | |
| Monomer DI-TMPTA | DI (TRIMETILOLPROPANA) TETRAAKRILAT | 94108-97-1 |
| Monomer akrilamida | ||
| ACMO Monomer | 4-akrilamorfolin | 5117-12-4 |
| Monomer di-fungsional | ||
| Monomer PEGDMA | Poli (etilen glikol) dimetakrilat | 25852-47-5 |
| Monomer TPGDA | Tripropilen glikol diakrilat | 42978-66-5 |
| Monomer TEGDMA | Trietilen glikol dimetakrilat | 109-16-0 |
| Monomer PO2-NPGDA | Propoksilat neopentilen glikol diakrilat | 84170-74-1 |
| Monomer PEGDA | Polietilen Glikol Diakrilat | 26570-48-9 |
| Monomer PDDA | Ftalat dietilen glikol diakrilat | |
| Monomer NPGDA | Neopentil glikol diakrilat | 2223-82-7 |
| Monomer HDDA | Hexamethylene Diacrylate | 13048-33-4 |
| Monomer EO4-BPADA | TERETOKSILASI (4) BISPHENOL A DIAKRILAT | 64401-02-1 |
| Monomer EO10-BPADA | TERETOKSILASI (10) BISPHENOL A DIAKRILAT | 64401-02-1 |
| Monomer EGDMA | Etilen glikol dimetakrilat | 97-90-5 |
| Monomer DPGDA | Dipropilen Glikol Dienoat | 57472-68-1 |
| Monomer Bis-GMA | Bisphenol A Glisidil Metakrilat | 1565-94-2 |
| Monomer Trifungsional | ||
| Monomer TMPTMA | Trimetilolpropana trimetakrilat | 3290-92-4 |
| Monomer TMPTA | Triakrilat trimetilolpropana | 15625-89-5 |
| PETA Monomer | 3524-68-3 | |
| GPTA (G3POTA) Monomer | GLISERIL PROPOKSI TRIAKRILAT | 52408-84-1 |
| Monomer EO3-TMPTA | Triakrilat trimetilolpropana teretoksilasi | 28961-43-5 |
| Monomer Fotoresis | ||
| IPAMA Monomer | 2-isopropil-2-adamantil metakrilat | 297156-50-4 |
| Monomer ECPMA | 1-Etilsiklopentil Metakrilat | 266308-58-1 |
| Monomer ADAMA | 1-Adamantil Metakrilat | 16887-36-8 |
| Monomer metakrilat | ||
| Monomer TBAEMA | 2- (Tert-butilamino) etil metakrilat | 3775-90-4 |
| Monomer NBMA | n-Butil metakrilat | 97-88-1 |
| MEMA Monomer | 2-Metoksietil Metakrilat | 6976-93-8 |
| Monomer i-BMA | Isobutil metakrilat | 97-86-9 |
| Monomer EHMA | 2-Etilheksil metakrilat | 688-84-6 |
| Monomer EGDMP | Etilen glikol Bis (3-merkaptopropionat) | 22504-50-3 |
| Monomer EEMA | 2-etoksietil 2-metilprop-2-enoat | 2370-63-0 |
| Monomer DMAEMA | N, M-Dimetilaminoetil metakrilat | 2867-47-2 |
| DEAM Monomer | Dietilaminoetil metakrilat | 105-16-8 |
| Monomer CHMA | Sikloheksil metakrilat | 101-43-9 |
| BZMA Monomer | Benzil metakrilat | 2495-37-6 |
| Monomer BDDMP | 1,4-Butanediol Di (3-merkaptopropionat) | 92140-97-1 |
| Monomer BDDMA | 1,4-Butanedioldimetakrilat | 2082-81-7 |
| Monomer AMA | Alil metakrilat | 96-05-9 |
| AAEM Monomer | Asetilasetoksietil metakrilat | 21282-97-3 |
| Monomer Akrilat | ||
| IBA Monomer | Isobutil akrilat | 106-63-8 |
| Monomer EMA | Etil metakrilat | 97-63-2 |
| Monomer DMAEA | Dimetilaminoetil akrilat | 2439-35-2 |
| DEAEA Monomer | 2- (dietilamino) etil prop-2-enoat | 2426-54-2 |
| CHA Monomer | sikloheksil prop-2-enoat | 3066-71-5 |
| BZA Monomer | benzil prop-2-enoat | 2495-35-4 |