사포닌은 아글리콘이 트리테르펜 또는 스테란 화합물인 배당체의 일종입니다. 인삼, 감초, 마 등 많은 한약재의 유효 성분 중 하나입니다(주요 사포닌 구조는 그림 1에 나와 있습니다). 면역력 및 기타 기능 강화. 문헌에는 진세노사이드의 생체 변환에 대한 많은 보고가 있습니다. 현재 150종 이상의 진세노사이드가 분리 및 동정되었습니다. 진세노사이드 Rb1, Rb2, Rc, Rd, Re 및 Rg1의 함량은 80%로 높은 반면 진세노사이드 Rg3, Rh2, F2 및 컴파운드 K (C-K) 및 기타 희귀 사포닌의 함량은 거의 없거나 전혀 없습니다. 연구에 따르면 일부 희귀 사포닌은 약리 활성이 좋은 것으로 나타났습니다. 그러나 함량이 낮기 때문에 제조 및 생산이 제한됩니다. 동일한 유형의 진세노사이드는 동일한 아글리콘을 가지고 있지만 설탕 사슬은 다릅니다. 희귀 진세노사이드와 같은 유형의 사포닌 함량이 높은 사포닌은 종종 2 ~ 3 개의 당 그룹 만 다릅니다. 따라서 고함량 사포닌의 효소 가수분해로 동일한 유형의 활성 희귀 사포닌을 제조할 수 있습니다.
Quick answer: A practical enzyme or food-ingredient decision starts with the process target, then checks activity, application window, sensory impact, and batch-to-batch consistency before scale-up.
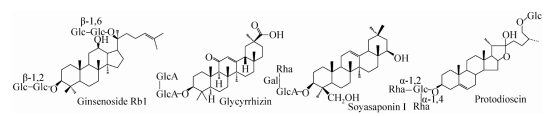
그림 1. 주요 사포닌의 구조
글리코사이드 가수분해효소마다 선택성이 다르며 진세노사이드를 가수분해하는 경로도 다릅니다. 표 1에서 볼 수 있듯이 다양한 글리코사이드 가수분해효소를 사용하여 다양한 희귀 진세노사이드를 제조할 수 있습니다. 진세노사이드 Rd는 진세노사이드 Rb1, Rb2, Rb3 및 Rc의 C-20 외부 당기를 가수분해하여 제조할 수 있습니다. 중국 백옥 달팽이와 써머스 칼도필러스에서 분리 및 정제된 β-글루코시다아제는 진세노사이드 Rb1을 Rd로 전환할 수 있습니다. 김 교수팀은 분자 복제 기술을 이용해 토양 미생물로부터 진세노사이드 Rb1을 Rd의 재조합 배당체 가수분해효소로 전환하는 기술을 확보했다. 이후 연구진은 써모토가 써마룸과 비피도박테리움 롱검 H-1에서 글루코시다제를 복제하여 진세노사이드 Rd의 변환 및 제조 효율을 향상시켰습니다. 재조합 기술로 플라보박테리움 존소니아와 써무스 써모필러스에서 얻은 글루코시다제는 진세노사이드 Rb1을 Rd로 전환할 뿐만 아니라 지페노사이드 XVII(G17)의 C-20 당쇄를 가수분해하여 진세노사이드 F2를 생성할 수 있습니다. 글루코시다제 외에도 진세노사이드 Rc를 Rd로 전환할 수 있는 α-L- 아라비노푸라노사이드 하이드롤라제는 인삼 뿌리에서, α-L- 아라비노푸라노사이드 하이드롤라제 및 α-L- 아라비노피라노사이드 하이드롤라제는 비피도박테리움 브레브와 비피도박테리움 롱검에서 얻어지며, 진세노사이드 Rc 및 Rb2를 Rd로 전환할 수 있습니다. 문헌에 따르면 칼디셀룰로시럽토 사카롤리티쿠스와 로다노박터 진세노시디무탄스의 α-L-알라비노푸라노사이드 가수분해효소는 진세노사이드 Rc를 Rd로 가수분해할 뿐만 아니라 화합물 Mc1(C-Mc1)을 F2로 전환할 수 있다고 보고되어 있습니다. Yu 등이 아스퍼질러스에서 분리 및 정제한 글리코사이드 가수분해효소는 모든 진세노사이드 Rb1, Rb2, Rb3 및 Rc를 Rd로 전환할 수 있습니다. 일부 글리코사이드 가수분해효소는 글리콜형 진세노사이드 Rb1, Rb2, Rb3, Rc 및 Rd와 같은 분자의 C-20 위치에서 당쇄를 완전히 가수분해하여 진세노사이드 Rg3를 생성할 수 있어 Rg3의 대량 생산이 가능하고 항암제 약물로 개발되고 있습니다. 고초균과 마이크로박테리움 에스테라로마티쿰의 글루코시다제는 진세노사이드 Rb1을 직접 가수분해하여 Rg3로 만들 수 있고, 마이크로박테리움 에스테라로마티쿰에서 분리 및 정제된 글루코시다제는 진세노사이드 Rb2를 가수분해하여 Rg3로 만들 수 있습니다. 분자 복제 기술로 슈도노카르디아에서 복제된 재조합 글리코사이드 가수분해효소는 진세노사이드 Rb1, Rb3 및 Rd를 변형하여 Rg3를 제조할 수 있습니다. 마찬가지로, 진세노사이드의 C-3 위치에서 당기를 가수분해하여 일련의 활성 희귀 진세노사이드를 제조할 수 있습니다. 스핑고모나스와 스핑고펙시스 알라스켄시스에서 복제된 재조합 글루코시다아제는 진세노사이드 Rb1, Rb2, Rc, Rd 및 Rg3 분자의 C-3 위치에서 당쇄 외부의 포도당을 가수분해하여 G17, 화합물 O(CO) 및 C-Mc1, F2 및 Rh2를 제조할 수 있습니다. 일부 글리코시다아제는 C-3 위치에서 내부 글루코실기를 직접 가수분해할 수 있습니다. 예를 들어, 테라박터 진세노시디무탄스와 에스테야 버미콜라의 글루코시다제는 진세노사이드 Rb1, Rb2, Rb3, Rc 및 Rd 분자의 C-3 위치에서 당쇄를 가수분해하여 해당 사포닌 LXXV(G75), 화합물 Y(C-Y), 화합물 Mx(C-Mx), 화합물 Mc(C-Mc) 및 C-K를 생성할 수 있습니다. 또한 일부 배당체 가수분해효소는 글리콜형 진세노사이드의 C-20 및 C-3 당 그룹을 동시에 가수분해할 수 있습니다. 아트로박터 클로로페놀리쿠스에서 복제된 재조합 글루코시다아제는 진세노사이드 Rb1, Rb2 및 Rc를 F2로 전환할 수 있습니다. 푸소박테리움 K60, 내생 진균 GE 17-18, 설폴로부스 아시도칼다리우스, 아스퍼질러스 니거, 마이크로박테리우 에스테라로마티움의 글리코사이드 가수분해효소는 진세노사이드 Rb1을 가수분해하여 C-K를 생성할 수 있습니다.
표 1. 글리코시다아제에 의한 진세노사이드의 생체 변환
| 제품 | 기판 | 반응 | 유기체 |
| Rd | Rb1 | β-글루코시다제 | 중국 백옥 달팽이 |
| Rd | Rb1 | β-글루코시다제 | Thermus 칼도필러스 |
| Rd | Rb1 | β-글루코시다제 | 배양되지 않은 박테리아 |
| Rd | Rb1 | β-글루코시다제 | 써모토가 써마럼 |
| Rd | Rb1 | β-글루코시다제 | 비피도박테리움 longum H-1 |
| Rd | Rb1 | β-글루코시다제 | 플라보박테리움 johnsoniae |
| Rd | Rb1 | β-글루코시다제 | Thermus 써모필루스 |
| Rd | Rb1 | β-글루코시다제 | 페니실륨 옥살리쿰 |
| Rd | Rb1 | β-글루코시다제 | 클라도스포리움 풀붐 |
| Rd | Rc | α-L-아라비노푸라노시다아제 | 파낙스 인삼 |
| Rd | Rc | α-L-아라비노푸라노시다아제 | 류코노스톡 |
| Rd | Rc | α-L-아라비노푸라노시다아제 | 비피도박테리움 브레브 |
| Rd | Rc | α-L-아라비노푸라노시다아제 | 비피도박테리움 longum |
| Rd | Rc | α-L-아라비노푸라노시다아제 | 칼디셀룰로시럽터 사카롤리티쿠스 |
| Rd | Rc | α-L-아라비노푸라노시다아제 | 로다노박터 진세노시디무탄 |
| Rd | Rb2 | α-L-아라비노피라노시다아제 | 비피도박테리움 브레브 |
| Rd | Rb2 | α-L-아라비노피라노시다아제 | 비피도박테리움 longum |
| Rd | Rb1/Rb2/Rb3/Rc | 글리코시다제 | 아스페르길루스 |
| Rg3 | Rb1 | β-글루코시다제 | 페실로마이세스 베이니어 |
| Rg3 | Rb1 | β-글루코시다제 | 미생물 에스테라로마티쿰 |
| Rg3 | Rb2 | β-글루코시다제 | 미생물 에스테라로마티쿰 |
| Rg3 | Rb1/Rb3/Rd | β-글루코시다제 | 가성 심근증 |
| G17 | Rb1 | β-글루코시다제 | 스핑고모나스 |
| G17 | Rb1 | β-글루코시다제 | 스핑고픽시스 알래스켄시스 |
| G17 | Rb1 | β-글루코시다제 | 셀룰로시 미생물 셀룰란 |
| G75 | Rb1 | β-글루코시다제 | 테라박터 진세노시디무탄 |
| G75 | Rb1 | β-글루코시다제 | Esteya 버미콜라 |
| F2 | G17 | β-글루코시다제 | 플라보박테리움 johnsoniae |
| F2 | G17 | β-글루코시다제 | Thermus 써모필루스 |
| F2 | C-Mc1 | α-L-아라비노푸라노시다아제 | 칼디셀룰로시럽터 사카롤리티쿠스 |
| F2 | C-Mc1 | α-L-아라비노푸라노시다아제 | 로다노박터 진세노시디무탄 |
| F2 | Rd | β-글루코시다제 | 셀룰로시 미생물 셀룰란 |
| F2 | Rb1/Rb2/Rc | β-글루코시다제 | 아트로박터 클로로페놀릭 |
| Rh2 | Rg3 | β-글루코시다제 | 스핑고픽시스 알래스켄시스 |
| CK | Rd | β-글루코시다제 | 테라박터 진세노시디무탄 |
| CK | Rd | β-글루코시다제 | Esteya 버미콜라 |
| CK | Rb1 | β-글루코시다제 | 푸소박테리움 K-60 |
| CK | Rb1 | β-글루코시다제 | 내생성 곰팡이 GE 17-18 |
| CK | Rb1/Rb2 | β-글루코시다제 | 설폴로버스 산도칼다리우스 |
| CK | Rb1/Rb2/Rb3/Rc | β-글루코시다제 | 아스페르길루스 niger |
| CK | Rb1/Rb2 | β-글루코시다제 | 마이크로박테리우 에스테라로마티쿰 |
| C-O | Rb2 | β-글루코시다제 | 셀룰로시 미생물 셀룰란 |
| C-Y | Rb2 | β-글루코시다제 | 테라박터 진세노시디무탄 |
| C-Mc | Rc | β-글루코시다제 | 테라박터 진세노시디무탄 |
| C-Mc1 | Rc | β-글루코시다제 | 셀룰로시 미생물 셀룰란스 |
| C-Mx | Rb3 | β-글루코시다제 | 테라박터 진세노시디무탄 |
| Rg2 | Re | β-글루코시다제 | 마이크로박테리움 에스테라로마티쿰 |
| Rg2 | Re | β-글루코시다제 | 뮤실라기니박터 |
| Rg2 | Re | β-글루코시다제 | 가성 심근증 |
| Rh1 | Rg1 | β-글루코시다제 | 마이크로박테리움 에스테라로마티쿰 |
| Rh1 | Rf | β-글루코시다제 | 파이로코커스 퓨리오수스 |
| Rh1 | Rf | β-글루코시다제 | 아스페르길루스 니거 |
| Rh1 | Rg2 | α-L-람노시다제 | 앱시디아 |
| Rh1 | R2 | β-자일로시다제 | 써모나에로박테리아 |
| F1 | Rg1 | β-글루코시다제 | 푸사리움 모닐리포르메 |
| F1 | Rg1 | β-글루코시다제 | 페니실륨 경화증 |
| F1 | Rg1 | β-글루코시다제 | 상귀박테리아 케디ii |
G17: 지페노사이드 XVII; G75: 지페노사이드 LXXV; C-O: 화합물 O; C-Y: 화합물 Y; C-Mc1: 화합물 Mc1; C-Mc: 화합물 Mc; C-Mx: 화합물 Mx; C-K: 화합물 K입니다.
트리올 진세노사이드의 C-6 및 C-20 당 그룹은 글리코사이드 가수분해 효소에 의해 가수분해될 수도 있습니다. 진세노사이드 Rg2는 글리코시다아제에 의해 Re 분자의 C-20 포도당을 가수분해하여 얻을 수 있습니다. 마이크로박테리움 에스테라로마티쿰, 뮤실라지니박터, 슈도노카르디아에서 복제된 재조합 글루코시다제는 진세노사이드 Re를 Rg2로 전환할 뿐만 아니라 진세노사이드 Rg1도 Rh1로 전환할 수 있습니다. 진세노사이드 Rf, Rg2 및 R2의 C-6 위치 밖에 있는 포도당, 람노스 및 자일로스는 모두 Rh1로 전환되어 Rh1을 제조할 수 있습니다. 진세노사이드 Rh1과 달리 진세노사이드 F1은 아글리콘의 C-20 위치에 포도당이 하나만 붙어 있습니다. 푸사리움 모닐리포르메, 페니실륨 스클레로티오룸, 상기박터 케디에이의 글루코시다제는 진세노사이드 Rg1의 C-6 포도당을 특이적으로 가수분해하여 진세노사이드 F1을 생성할 수 있습니다.
글리코사이드 가수분해효소는 활성 희귀 진세노사이드를 변형하고 제조하는 데 사용될 뿐만 아니라 감초, 콩, 마 등의 사포닌을 가수분해하고 변형하는 데도 널리 사용됩니다(표 2). 스트렙토코커스 LJ-22 및 페니실리움 푸르푸로제눔 Li-3에서 분리 및 정제된 글루쿠로니다제는 글리시리진을 가수분해하여 모노글루쿠론산 글리시리진을 생성할 수 있으며 부산물 글리시레틴산은 없습니다. 모라나 등은 아스퍼질러스 니거에서 추출한 글루쿠로니다제를 사용하여 글리시리진을 완전히 가수분해하여 글리시레틴산을 생산했습니다. 아스퍼질러스 오리제에서 분리 및 정제된 소야사포닌 가수분해효소는 소야사포닌 I을 가수분해하여 소야사포놀 B를 생산할 수 있으며, 네오코스모스포라 바신페타의 새로운 소야사포닌 가수분해효소는 대두 사포닌 I, II, III을 대두 사포닌 B로 전환하여 항산화 및 혈액 지질 조절 기능을 가진 대두 사포닌을 제조하는 데 효과적인 도구를 제공할 수 있습니다. 스테로이드 사포닌 중에서도 디오스신의 당쇄의 가수분해 변형에 대한 연구와 비교는 체계적으로 이루어지고 있습니다. 이노우에 등은 원래 디오스게닌을 가수분해하여 디오스게닌을 생산할 수 있는 글루코시다제를 코스투스 스펙시오수스에서 분리 및 정제했습니다. Liu 등은 아스퍼질러스 오리제(Aspergillus oryzae)에서 분리, 정제 및 복제하여 재조합 디오스신 가수분해효소를 얻어 디오스신의 글루코실과 α-1,4 람노실기를 가수분해하여 디오스신 III를 생산할 수 있습니다. Feng 등이 Curvularia lunata에서 분리 및 정제 한 α-L- 람노시다 제는 디오 신의 α-1,2 람노 실기를 가수 분해하여 디오 신 V를 생성 할 수 있습니다. Qian 등은 신선한 쇠고기 간에서 α-L- 람노시다 제를 분리 및 정제하여 α-1,2 및 α-1,4 두 람노 실기를 가수 분해하여 포도당 그룹을 형성 할 수있는 디오 제닌을 분리 및 정제했습니다. -디오스게닌. Fu 등은 디오스게닌을 디오스게닌으로 완전히 가수분해할 수 있는 앱시디아에서 디오스게닌 가수분해효소를 분리 및 정제했습니다.
표 2. 글리코시다아제에 의한 다른 사포닌의 생체 변환
| 제품 | 기판 | 반응 | 유기체 |
| GAMG | 글리시리진 | β-글루쿠로니다아제 | 스트렙토코커스 |
| GAMG | 글리시리진 | β-글루쿠로니다아제 | 페니실륨 푸르푸로제넘 |
| 글리시레틴산 | 글리시리진 | β-글루쿠로니다아제 | 아스페르길루스 니거 |
| 소야사포제놀 B | 소야사포닌 I | 대두 사포닌 가수분해 효소 | 아스페르길루스 오리제 |
| 소야사포제놀 B | 소야사포닌 | 대두 사포닌 가수분해 효소 | 네오코스모스포라 혈관감염증 |
| 디오스킨 | 프로토디오신 | β-글루코시다제 | Costus speciosus |
| 프로제닌 III | 프로토디오신 | 프로토디오신-글리코시다제 | 아스페르길루스 오리제 |
| 프로제닌 V | 디오스킨 | α-L-람노시다제 | 커뷸라리아 루나타 |
| 디오스제닐-글루코사이드 | 디오스킨 | α-L-람노시다제 | 소 간 |
| 디오스제닌 | 디오스킨 | 디오신-글리코시다제 | 앱시디아 |
GAMG: 글리시르산 모노글루쿠로니드
A practical sourcing checklist for enzyme, biotech, and food-ingredient topics
In enzyme and food-processing projects, the most useful decision frame is usually application fit plus process stability: which ingredient performs under the intended pH, temperature, time, and substrate conditions without creating a downstream quality or compliance problem.
- Define the processing target first: flavor, hydrolysis, texture, fermentation, cleaning, and bioprocess applications often need very different activity profiles.
- Check the real operating window: pH, temperature, residence time, and substrate type often matter more than a headline product claim.
- Review consistency and downstream impact: dosage, sensory influence, filtration, and shelf-life behavior can all affect the final commercial value.
- Use pilot validation: small production tests usually reveal the most useful differences in activity, efficiency, and process fit.
Recommended product references
- Longzyme Lipase: A direct product reference for lipase-related food, cleaning, or bioprocess discussions.
- Longzyme Beta-Amylase: A practical enzyme reference when starch conversion and food-processing activity are under review.
- Longzyme Compound Glucoamylase: A useful enzyme reference when saccharification or related processing performance matters.
- 효모 추출물: A practical ingredient reference when flavor, fermentation, or nutrient-support applications are involved.
FAQ for buyers and formulators
Why is a high-activity enzyme not automatically the best commercial choice?
Because the best enzyme is the one that performs reliably under the actual process conditions and gives the desired downstream result without creating new issues.
Should food and biotech ingredients be selected from data sheets alone?
It is usually safer to pair the specification review with a pilot or application test because real substrates and process windows can change the result a lot.
지금 문의하세요!
가격이 필요한 경우 아래 양식에 연락처 정보를 입력해 주시면 보통 24시간 이내에 연락드리겠습니다. 이메일을 보내셔도 됩니다. info@longchangchemical.com 근무 시간(오전 8시 30분~오후 6시, 월~토요일)에 문의하거나 웹사이트 라이브 채팅을 이용하면 신속하게 답변을 받을 수 있습니다.
| 복합 글루코아밀라아제 | 9032-08-0 |
| 풀룰라나아제 | 9075-68-7 |
| 자일라나제 | 37278-89-0 |
| 셀룰라아제 | 9012-54-8 |
| 나린기나제 | 9068-31-9 |
| β-아밀라아제 | 9000-91-3 |
| 포도당 산화 효소 | 9001-37-0 |
| 알파-아밀라아제 | 9000-90-2 |
| 펙티나아제 | 9032-75-1 |
| 과산화효소 | 9003-99-0 |
| 리파아제 | 9001-62-1 |
| 카탈라아제 | 9001-05-2 |
| 탄나세 | 9025-71-2 |
| 엘라스타제 | 39445-21-1 |
| Urease | 9002-13-5 |
| 덱스트라나제 | 9025-70-1 |
| L-락트 탈수소 효소 | 9001-60-9 |
| 탈수소 효소 말레이트 | 9001-64-3 |
| 콜레스테롤 산화 효소 | 9028-76-6 |
