A szaponinok a glikozidok egy olyan osztálya, amelyben az aglikonok triterpén- vagy szteránvegyületek. Ezek számos kínai növényi gyógyszer, például a ginzeng, az édesgyökér és a jamgyökér egyik hatékony összetevője (a fő szaponinok szerkezetét az 1. ábra mutatja). Fokozzák az immunitást és más funkciókat. Az irodalomban számos jelentés található a ginzenozidok biotranszformációjáról. Jelenleg több mint 150 féle ginzenozidot különítettek el és azonosítottak. A ginzenozidok Rb1, Rb2, Rc, Rd, Re és Rg1 tartalma eléri a 80%-t, míg a ginzenozidok Rg3, Rh2, F2 és Compound K (C-K) és más ritka szaponinok tartalma kevés vagy egyáltalán nincs. Tanulmányok kimutatták, hogy néhány ritka szaponin jó farmakológiai aktivitással rendelkezik. Az alacsony tartalom miatt azonban a készítmény előállítása és termelése korlátozott. Az azonos típusú ginzenozidoknak ugyanaz az aglikonjuk, de a cukroláncuk eltérő. A ritka ginzenozidok és az azonos típusú szaponinok magasabb tartalma gyakran csak 2-3 cukorcsoportban különbözik. Ezért a magas szaponin-tartalmú szaponin enzimatikus hidrolízisével azonos típusú aktív ritka szaponin állítható elő.
Quick answer: A practical enzyme or food-ingredient decision starts with the process target, then checks activity, application window, sensory impact, and batch-to-batch consistency before scale-up.
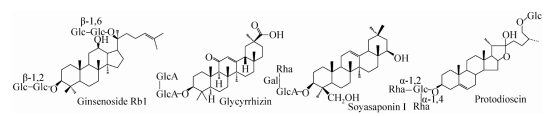
1. ábra. A fő szaponinok szerkezete
A különböző glikozid-hidrolázok különböző szelektivitással rendelkeznek, és a ginzenozidok hidrolízisének útjai is eltérőek. Amint az 1. táblázatban látható, különböző glikozid-hidrolázok különböző ritka ginzenozidok előállítására használhatók. Az Rd ginzenozidot az Rb1, Rb2, Rb3 és Rc ginzenozidok C-20 külső cukorcsoportjának hidrolízisével lehet előállítani. A kínai fehér jáde csigából és Thermus caldophilusból izolált és tisztított β-glükozidáz képes az Rb1 ginzenozidot Rd-vé alakítani. Kim és munkatársai talajmikroorganizmusokból nyerték molekuláris klónozási technológiával a ginzenozid Rb1 átalakítására, amely a Rd rekombináns glikozid-hidroláza. Ezt követően a kutatók Thermotoga thermarumból és Bifidobacterium longum H-1-ből klónoztak glükozidázt, ami javította a ginzenozid Rd átalakításának és előállításának hatékonyságát. A Flavobacterium johnsoniae-ből és Thermus thermophilusból rekombináns technológiával nyert glükozidáz nemcsak a ginzenozid Rb1-et képes Rd-vé alakítani, hanem a ginzenozid XVII (G17) C-20 cukroláncát is hidrolizálja, hogy ginzenozid F2-t állítson elő. A glükozidáz mellett a ginzenozid Rc-t Rd-vé alakítani képes α-L-arabinofuranozid-hidrolázt ginzenggyökérből és Leuconostoc sp. A Bifidobacterium breve és Bifidobacterium longum fajokból nyerték az α-L-arabinofuranozid-hidrolázt és az α-L-arabinopiranozid-hidrolázt, amelyek a ginzenozid Rc-t és Rb2-t Rd-vé képesek átalakítani. Az irodalomban arról számoltak be, hogy a Caldicellulosiruptor saccharolyticus és a Rhodanobacter ginsenosidimutans α-L-arabinofuranozid-hidroláza nemcsak a ginsenozid Rc-t képes Rd-vé hidrolizálni, hanem az Mc1 vegyületet (C-Mc1) is F2-vé alakítja. A Yu és munkatársai által Aspergillusból izolált és tisztított glikozid-hidroláz képes az összes Rb1, Rb2, Rb3 és Rc ginzenozidot Rd-vé alakítani. Néhány glikozid-hidroláz képes teljesen hidrolizálni a C-20 pozícióban lévő cukroláncokat a molekulákban, mint például az Rb1, Rb2, Rb3, Rc és Rd glikol típusú ginzenozidokban, hogy létrehozza az Rg3 ginzenozidot, amely lehetővé teszi az Rg3 nagyüzemi előállítását, és amelyet daganatellenes hatóanyagként fejlesztettek ki. A Paecilomyces bainier és a Microbacterium esteraromaticum glükozidáza képes a ginzenozid Rb1-et közvetlenül Rg3-á hidrolizálni, míg a Microbacterium esteraromaticumból izolált és tisztított glükozidáz képes a ginzenozid Rb2-t Rg3-á hidrolizálni. A Pseudonocardiából molekuláris klónozási technológiával klónozott rekombináns glikozid-hidroláz képes az Rb1, Rb3 és Rd ginzenozidokat átalakítani az Rg3 előállításához. Hasonlóképpen, egy sor aktív ritka ginzenozidot lehet előállítani a ginzenozidok C-3 pozíciójában lévő cukorcsoport hidrolízisével. A Sphingomonasból és Sphingopyxis alaskensisből klónozott rekombináns glükozidáz képes hidrolizálni a ginzenozid Rb1, Rb2, Rc, Rd és Rg3 molekulákban a C-3 pozícióban lévő cukorláncon kívüli glükózt, és előállítani a G17, az O vegyületet (CO), valamint a C-Mc1, F2 és Rh2 molekulákat. Egyes glikozidázok közvetlenül hidrolizálni tudják a C-3 pozícióban lévő belső glükozilcsoportot. Például a Terrabacter ginsenosidimutans és az Esteya vermicola glükozidáza képes hidrolizálni a ginsenozid Rb1, Rb2, Rb3, Rc és Rd molekulák C-3 pozíciójában lévő cukroláncot, hogy előállítsa a megfelelő szaponin LXXV (G75), Y vegyület (C-Y), Mx vegyület (C-Mx), Mc vegyület (C-Mc) és C-K vegyületet. Ezenkívül egyes glikozid-hidrolázok képesek egyidejűleg hidrolizálni a glikol típusú ginzenozidok C-20 és C-3 cukorcsoportjait. Az Arthrobacter chlorophenolicusból klónozott rekombináns glükozidáz képes az Rb1, Rb2 és Rc ginzenozidokat F2-vé alakítani. A Fusobacterium K60-ban, a GE 17-18 endofita gombákban, a Sulfolobus acidocaldariusban, az Aspergillus nigerben és a Microbacteriu esteraromaticumban található glikozid-hidroláz képes hidrolizálni a ginzenozid Rb1-et C-K előállítására.
1. táblázat. A ginzenozidok glikozidáz általi biotranszformációja
| Termék | Alátét | Reakció | Szervezet |
| Rd | Rb1 | β-glükozidáz | Kína fehér jáde csiga |
| Rd | Rb1 | β-glükozidáz | Thermus caldophilus |
| Rd | Rb1 | β-glükozidáz | Kitenyésztetlen baktériumok |
| Rd | Rb1 | β-glükozidáz | Thermotoga thermarum |
| Rd | Rb1 | β-glükozidáz | Bifidobacterium longum H-1 |
| Rd | Rb1 | β-glükozidáz | Flavobacterium johnsoniae |
| Rd | Rb1 | β-glükozidáz | Thermus thermophilus |
| Rd | Rb1 | β-glükozidáz | Penicillium oxalicum |
| Rd | Rb1 | β-glükozidáz | Cladosporium fulvum |
| Rd | Rc | α-L-Arabinofuranozidáz | Panax ginseng |
| Rd | Rc | α-L-Arabinofuranozidáz | Leuconostoc |
| Rd | Rc | α-L-Arabinofuranozidáz | Bifidobacterium breve |
| Rd | Rc | α-L-Arabinofuranozidáz | Bifidobacterium longum |
| Rd | Rc | α-L-Arabinofuranozidáz | Caldicellulosiruptor saccharolyticus |
| Rd | Rc | α-L-Arabinofuranozidáz | Rhodanobacter ginsenosidimutans |
| Rd | Rb2 | α-L-Arabinopiranozidáz | Bifidobacterium breve |
| Rd | Rb2 | α-L-Arabinopiranozidáz | Bifidobacterium longum |
| Rd | Rb1/Rb2/Rb3/Rc | Glikozidáz | Aspergillus |
| Rg3 | Rb1 | β-glükozidáz | Paecilomyces bainier |
| Rg3 | Rb1 | β-glükozidáz | Microbacterium esteraromaticum |
| Rg3 | Rb2 | β-glükozidáz | Microbacterium esteraromaticum |
| Rg3 | Rb1/Rb3/Rd | β-glükozidáz | Pseudonocardia |
| G17 | Rb1 | β-glükozidáz | Sphingomonas |
| G17 | Rb1 | β-glükozidáz | Sphingopyxis alaskensis |
| G17 | Rb1 | β-glükozidáz | Cellulosimicrobium cellulánok |
| G75 | Rb1 | β-glükozidáz | Terrabacter ginsenosidimutans |
| G75 | Rb1 | β-glükozidáz | Esteya vermicola |
| F2 | G17 | β-glükozidáz | Flavobacterium johnsoniae |
| F2 | G17 | β-glükozidáz | Thermus thermophilus |
| F2 | C-Mc1 | α-L-Arabinofuranozidáz | Caldicellulosiruptor saccharolyticus |
| F2 | C-Mc1 | α-L-Arabinofuranozidáz | Rhodanobacter ginsenosidimutans |
| F2 | Rd | β-glükozidáz | Cellulosimicrobium cellulánok |
| F2 | Rb1/Rb2/Rc | β-glükozidáz | Arthrobacter chlorophenolicus |
| Rh2 | Rg3 | β-glükozidáz | Sphingopyxis alaskensis |
| CK | Rd | β-glükozidáz | Terrabacter ginsenosidimutans |
| CK | Rd | β-glükozidáz | Esteya vermicola |
| CK | Rb1 | β-glükozidáz | Fusobacterium K-60 |
| CK | Rb1 | β-glükozidáz | endofita gombák GE 17-18 |
| CK | Rb1/Rb2 | β-glükozidáz | Sulfolobus acidocaldarius |
| CK | Rb1/Rb2/Rb3/Rc | β-glükozidáz | Aspergillus niger |
| CK | Rb1/Rb2 | β-glükozidáz | Microbacteriu esteraromaticum |
| C-O | Rb2 | β-glükozidáz | Cellulosimicrobium cellulánok |
| C-Y | Rb2 | β-glükozidáz | Terrabacter ginsenosidimutans |
| C-Mc | Rc | β-glükozidáz | Terrabacter ginsenosidimutans |
| C-Mc1 | Rc | β-glükozidáz | Cellulosimicrobium cellulans |
| C-Mx | Rb3 | β-glükozidáz | Terrabacter ginsenosidimutans |
| Rg2 | Re | β-glükozidáz | Microbacterium esteraromaticum |
| Rg2 | Re | β-glükozidáz | Mucilaginibacter |
| Rg2 | Re | β-glükozidáz | Pseudonocardia |
| Rh1 | Rg1 | β-glükozidáz | Microbacterium esteraromaticum |
| Rh1 | Rf | β-glükozidáz | Pyrococcus furiosus |
| Rh1 | Rf | β-glükozidáz | Aspergillus niger |
| Rh1 | Rg2 | α-L-Ramnosidáz | Absidia |
| Rh1 | R2 | β-Xilozidáz | Thermoanaerobacterium |
| F1 | Rg1 | β-glükozidáz | Fusarium moniliforme |
| F1 | Rg1 | β-glükozidáz | Penicillium sclerotiorum |
| F1 | Rg1 | β-glükozidáz | Sanguibacter keddieii |
G17: XVII. gypenozid; G75: LXXV. gypenozid; C-O: O vegyület; C-Y: Y vegyület; C-Mc1: Mc1 vegyület; C-Mc: Mc vegyület; C-Mx: Mx vegyület; C-K: K vegyület.
A triol ginzenozidok C-6 és C-20 cukorcsoportjait glikozid-hidrolázok is hidrolizálhatják. A ginzenozid Rg2 a Re molekulában lévő C-20 glükóz glikozidázzal történő hidrolizálásával nyerhető. A Microbacterium esteraromaticumból, Mucillaginibacterből és Pseudonocardiából klónozott rekombináns glükozidáz nemcsak a ginzenozid Re-t képes Rg2-vé alakítani, hanem a ginzenozid Rg1 is Rh1-vé alakul. A ginzenozid Rf, Rg2 és R2 C-6 pozícióján kívüli glükóz, ramnóz és xilóz mind átalakítható Rh1 előállítására. A ginzenozid Rh1-től eltérően a ginzenozid F1 aglikonjának C-20 pozíciójához csak egy glükóz kapcsolódik. A Fusarium moniliforme, a Penicillium sclerotiorum és a Sanguibacter keddieii glükozidázai képesek specifikusan hidrolizálni a ginzenozid Rg1 C-6 glükózát, hogy ginzenozid F1-et állítsanak elő.
A glikozid-hidrolázt nemcsak az aktív ritka ginzenozidok átalakítására és előállítására használják, hanem széles körben használják a szaponinok, például az édesgyökér, a szójabab és a jamgyökér hidrolizálására és módosítására is (2. táblázat). A Streptococcus LJ-22-ből és a Penicillium purpurogenum Li-3-ból izolált és tisztított glükuronidáz képes hidrolizálni a glicirrizint monoglükuronsavas glicirrizint előállítani, és nincs melléktermék glicirretinsav. Morana és munkatársai Aspergillus nigerből származó glükuronidázt használtak a glicirrizin teljes hidrolíziséhez, hogy glicirretinsavat állítsanak elő. Az Aspergillus oryzae-ből izolált és tisztított szójaszaponin-hidroláz képes hidrolizálni a szójaszaponin I-et szójaszaponin B előállítására. A Neocosmospora vasinfecta-ban található új szójaszaponin-hidroláz képes a szójaszaponin I, II és III-t szójaszaponin B-vé alakítani, ami hatékony eszköz a szójaszaponin antioxidációs és vérzsír-szabályozó hatású előállításához. A szteroid szaponinok közül a dioszcin cukroláncának hidrolízis-módosításának kutatása és összehasonlítása szisztematikus. Inoue és munkatársai izoláltak és tisztítottak egy glükozidázt a Costus speciosusból, amely képes hidrolizálni az eredeti dioszgénint dioszgénin előállítására. Liu és munkatársai Aspergillus oryzae-ből izoláltak, tisztítottak és klónoztak egy rekombináns dioszcin-hidrolázt, amely képes hidrolizálni a dioszcin glükozil- és α-1,4 ramnozilcsoportjait dioszcin III előállítása céljából. A Feng és munkatársai által a Curvularia lunatából izolált és tisztított α-L-ramnozidáz képes hidrolizálni a diozcin α-1,2 ramnozilcsoportját, hogy diozcin V-t állítson elő. Qian és munkatársai friss marhamájból izoláltak és tisztítottak egy α-L-ramnozidázt, amely képes hidrolizálni a diozgénin α-1,2 és α-1,4 két ramnozilcsoportját glükózcsoportot képezve. -Diosgenin. Fu és munkatársai abszidiából izolálták és tisztították a dioszgenin-hidrolázt, amely képes a dioszgenint teljes mértékben dioszgeninné hidrolizálni.
2. táblázat. Egyéb szaponinok biotranszformációja glikozidázzal
| Termék | Alátét | Reakció | Szervezet |
| GAMG | Glycyrrhizin | β-Glikuronidáz | Streptococcus |
| GAMG | Glycyrrhizin | β-Glikuronidáz | Penicillium purpurogenum |
| Glicirretinsav | Glycyrrhizin | β-Glikuronidáz | Aspergillus niger |
| Szójaszapogenol B | Szójaszaponin I | Szójabab szaponin-hidroláz | Aspergillus oryzae |
| Szójaszapogenol B | Szójaszaponin | Szójabab szaponin-hidroláz | Neocosmospora vasinfecta |
| Dioscin | Protodioscin | β-glükozidáz | Costus speciosus |
| Progenin III | Protodioscin | Protodiozin-glikozidáz | Aspergillus oryzae |
| Progenin V | Dioscin | α-L-Ramnosidáz | Curvularia lunata |
| Dioszgenilglükozid | Dioscin | α-L-Ramnosidáz | Szarvasmarha-máj |
| Diosgenin | Dioscin | Dioszcin-glikozidáz | Absidia |
GAMG: glicirretikus sav-mono-glükuronid
A practical sourcing checklist for enzyme, biotech, and food-ingredient topics
In enzyme and food-processing projects, the most useful decision frame is usually application fit plus process stability: which ingredient performs under the intended pH, temperature, time, and substrate conditions without creating a downstream quality or compliance problem.
- Define the processing target first: flavor, hydrolysis, texture, fermentation, cleaning, and bioprocess applications often need very different activity profiles.
- Check the real operating window: pH, temperature, residence time, and substrate type often matter more than a headline product claim.
- Review consistency and downstream impact: dosage, sensory influence, filtration, and shelf-life behavior can all affect the final commercial value.
- Use pilot validation: small production tests usually reveal the most useful differences in activity, efficiency, and process fit.
Recommended product references
- Longzyme Lipase: A direct product reference for lipase-related food, cleaning, or bioprocess discussions.
- Longzyme Beta-Amylase: A practical enzyme reference when starch conversion and food-processing activity are under review.
- Longzyme Compound Glucoamylase: A useful enzyme reference when saccharification or related processing performance matters.
- Élesztő kivonat: A practical ingredient reference when flavor, fermentation, or nutrient-support applications are involved.
FAQ for buyers and formulators
Why is a high-activity enzyme not automatically the best commercial choice?
Because the best enzyme is the one that performs reliably under the actual process conditions and gives the desired downstream result without creating new issues.
Should food and biotech ingredients be selected from data sheets alone?
It is usually safer to pair the specification review with a pilot or application test because real substrates and process windows can change the result a lot.
Lépjen kapcsolatba velünk most!
Ha szüksége van Price-ra, kérjük, töltse ki elérhetőségét az alábbi űrlapon, általában 24 órán belül felvesszük Önnel a kapcsolatot. Ön is küldhet nekem e-mailt info@longchangchemical.com munkaidőben ( 8:30-18:00 UTC+8 H.-Szombat ) vagy használja a weboldal élő chatjét, hogy azonnali választ kapjon.
| Összetétel Glükoamiláz | 9032-08-0 |
| Pullulanase | 9075-68-7 |
| Xilanáz | 37278-89-0 |
| Celluláz | 9012-54-8 |
| Naringináz | 9068-31-9 |
| β-Amiláz | 9000-91-3 |
| Glükóz-oxidáz | 9001-37-0 |
| alfa-amiláz | 9000-90-2 |
| Pektináz | 9032-75-1 |
| Peroxidáz | 9003-99-0 |
| Lipáz | 9001-62-1 |
| Kataláz | 9001-05-2 |
| TANNASE | 9025-71-2 |
| Elasztáz | 39445-21-1 |
| Ureáz | 9002-13-5 |
| DEXTRANASE | 9025-70-1 |
| L-laktil-dehidrogenáz | 9001-60-9 |
| Dehidrogenáz malát | 9001-64-3 |
| Koleszterin-oxidáz | 9028-76-6 |
