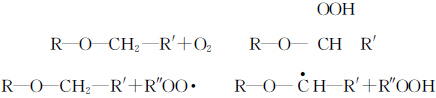Qual é o efeito do monômero UV no bloqueio de oxigênio curável por UV?
1.2 Preparação e teste de amostras
O monômero e o iniciador foram pesados com precisão, quando o monômero não foi purificado, e misturados uniformemente com um agitador magnético. A UV-DSC foi usada para realizar experimentos de cura por UV sob atmosfera de ar estático e atmosfera de nitrogênio, e as amostras foram coletadas em quantidades iguais a cada vez, de modo que a espessura das amostras no cadinho fosse a mesma. O programa UV-DSC foi configurado para manter a temperatura da amostra constante por 2 minutos e, em seguida, a fonte de luz foi ligada automaticamente pelo programa, e a luz UV (faixa de comprimento de onda de 325 a 400 nm) foi introduzida na célula DSC pela fibra de vidro para iluminar o cadinho da amostra e o cadinho de referência, e o DSC mediu o valor do fluxo de calor do processo de fotopolimerização da amostra. A intensidade da luz foi medida como 48,27 mW-cm-2. A intensidade da luz foi determinada espalhando-se negro de fumo no fundo do cadinho de amostra, e a energia absorvida pela luz foi medida pelo UV-DSC e dividida pela área do fundo do cadinho para obter a intensidade da luz.
2 Resultados e discussão
2.1 Processamento de dados
A taxa de fotopolimerização foi calculada como
A taxa de fotopolimerização R=dC/dt=(dH/dt)/Hmax, em que dH/dt é o valor do fluxo de calor na curva de entalpia versus tempo do processo de fotopolimerização medido por UV-DSC; Hmax é o calor total de polimerização da amostra em 200 s de exposição à luz, obtido pela integração do pico exotérmico da fotopolimerização. O tempo correspondente à taxa máxima de cura do processo de cura por luz é tmax. A polimerização de radicais livres ocorrerá automaticamente em um fenômeno acelerado, a curva da taxa de cura por luz para a derivada de tempo, o valor máximo da curva correspondente ao tempo registrado como tamax, esse tempo pode ser considerado o tempo de crescimento mais rápido da taxa de cura por luz, nesse momento o bloqueio de oxigênio do sistema e o efeito de gaiola e outros fatores no consumo de radicais primários são mínimos. O monômero iniciador de radical livre começa a se polimerizar rapidamente.
Cálculo do conteúdo do iniciador (fração molar) α na amostra:
Em que n iniciador é a quantidade molar de iniciador no sistema, f é o grau funcional do monômero e n monômero é a quantidade molar de monômero no sistema. A Figura 1 mostra a estrutura molecular do iniciador Irgacure-184, que é do tipo clivagem, e o "2" na fórmula (1) significa que uma molécula do iniciador pode, teoricamente, ser decomposta em duas moléculas de radicais pela exposição à luz.
A fórmula estrutural do Irgacure-184
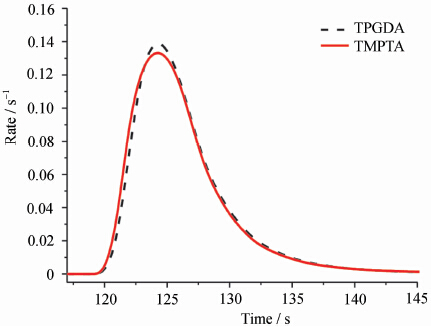
A Figura 2 mostra as curvas de taxa de cura por luz de diferentes monômeros com teor de iniciador 4% (fração de massa). Como pode ser visto na figura, para diferentes monômeros, há diferenças na taxa de cura no período de pré-cura, e essa diferença também é expressa em tempo, o que indica que a cura UV de diferentes monômeros apresenta diferenças de velocidade no tempo. O tempo tamax, quando a taxa de cura por luz do monômero cresce mais rapidamente, e o tempo tmax, correspondente à taxa máxima de cura por luz, são comparados com a curva de variação do conteúdo do iniciador, e os resultados são mostrados na Figura 3.
Curvas de taxa de cura por UV de diferentes monômeros com o iniciador 4%
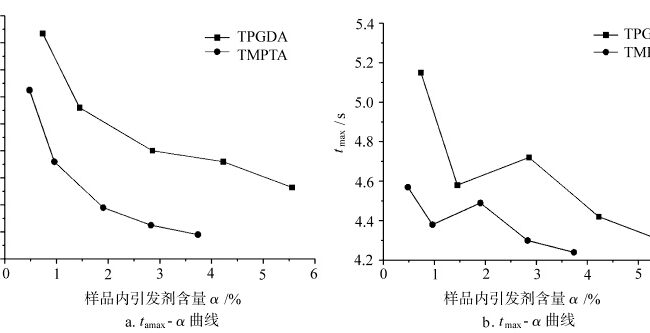
A relação de tmáximo e tmáximo com teores de iniciadores no processo de cura ao ar de diferentes monômeros
A Figura 3 mostra as curvas de tmax e tamax para a cura por luz de diferentes monômeros ao ar como uma função do teor de iniciador α na amostra. No estágio inicial da cura, quando o oxigênio está presente, parte dos radicais reativos gerados pelo fotoiniciador devido à luz é consumida pelo oxigênio dissolvido na amostra, e a outra parte inicia a polimerização do monômero. O efeito de bloqueio do oxigênio consome os radicais gerados pela decomposição do iniciador e dos radicais do monômero, afetando assim a magnitude do tamax e do tmax da fotopolimerização, o que, por sua vez, reflete a sensibilidade da fotopolimerização ao oxigênio e ao teor de iniciador. Conforme observado na Fig. 3a, o tamax da fotopolimerização de cada monômero diminui com o aumento do teor de iniciador em um determinado padrão. Na Fig. 3b, o tmax da fotopolimerização de cada monômero mostra uma certa flutuação com o aumento do teor de iniciador. Isso ocorre porque, quando a taxa de reação de cura atinge o máximo, o sistema atinge um alto grau de cura e os segmentos da cadeia molecular são gradualmente congelados devido ao efeito vítreo, e a sensibilidade do tmax da reação de fotopolimerização ao teor de iniciador é reduzida nesse momento. Enquanto o tamax, no estágio inicial da fotopolimerização, quando o sistema não apresenta alto grau de polimerização, a reação de fotopolimerização é mais sensível ao conteúdo do iniciador no sistema. Portanto, em comparação, o tamax reflete melhor a sensibilidade da fotopolimerização ao teor de iniciador.
2.2 Efeito da atmosfera no tamax de fotopolimerização de diferentes monômeros
Na atmosfera de ar, o tamax do material fotocurado deve ser diferente em comparação com o da atmosfera de nitrogênio devido ao efeito do bloqueio de oxigênio. Foram realizados testes de UV-DSC no monômero TMPTA em atmosfera de ar e nitrogênio quando foi adicionado um teor menor de iniciador, e os resultados estão listados na Tabela 1.
| tamaxtamax de cura UV de TMPTA com baixo teor de iniciador no ar ou N2 | ||
| Conteúdo do iniciador na amostra/% | tamax/s | |
| ar | N2 | |
| 0.48 | 2.65 | 2.18 |
| 0.96 | 2.12 | 1.92 |
tmáximo de cura UV do TMPTA com baixo teor de iniciador no ar ou em N2
A Tabela 1 mostra a comparação do tamax do TMPTA fotocurado ao ar e ao nitrogênio, respectivamente, com a adição de níveis mais baixos de iniciador. Na tabela acima, pode-se observar que o tamax da fotopolimerização ao ar é maior do que ao nitrogênio quando o teor de iniciador é igual, indicando que a fotopolimerização ao ar é afetada pelo bloqueio de oxigênio. Em geral, acredita-se que o oxigênio dissolvido na matéria-prima e na superfície sofre as seguintes reações durante o processo de fotopolimerização.
Os radicais de peróxido gerados ROO- são muito estáveis e não têm capacidade de iniciar reações de polimerização. O oxigênio não apenas elimina os radicais gerados pelo iniciador durante o processo de fotopolimerização, mas também termina os radicais do monômero.
A sensibilidade da fotocura à polimerização de bloqueio de oxigênio varia para diferentes monômeros e está relacionada a fatores como funcionalidades do monômero, atividade de ligação dupla e estrutura [13]. Para investigar o efeito da estrutura do monômero na agregação de bloqueio de oxigênio, dois TMPTAs EO-ized diferentes foram selecionados para experimentos de UV-DSC em condições de ar e nitrogênio, respectivamente. Todos esses monômeros homólogos têm estruturas semelhantes, exceto pelo número de grupos EO, o que evita complicar o problema escolhendo alguns outros monômeros com estruturas muito diferentes [13].
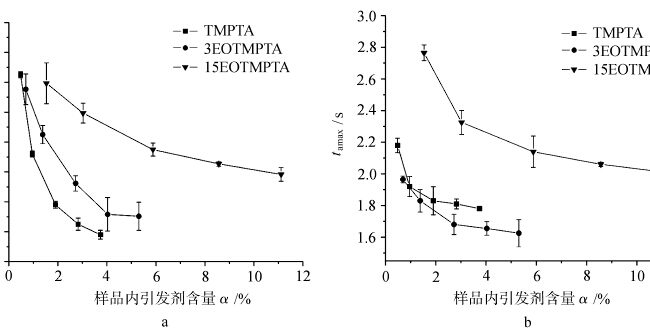
A Figura 4 mostra a variação do tamax com o teor de iniciador dentro da amostra para a fotopolimerização de monômeros TMPTA com diferentes EOizações sob ar e nitrogênio. Conforme observado na figura, o tamax de cada monômero fotopolimerizado com ar e nitrogênio diminui com o aumento do teor de iniciador. A variação do tamax fotopolimerizado de cada monômero sob ar e nitrogênio varia com a quantidade de EO no monômero. Isso mostra que a quantidade de EO no monômero tem um efeito sobre o tamax da cura por luz. Para o mesmo monômero, a diferença no tamax de cura por luz sob ar e nitrogênio está relacionada à barreira de oxigênio quando as outras condições são as mesmas.
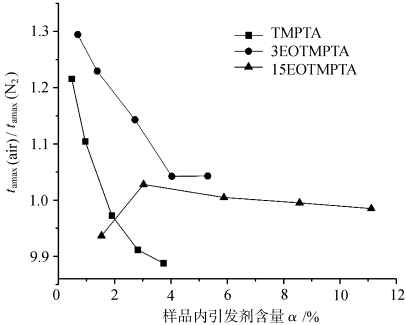
A Figura 5 mostra as curvas da proporção de tamax de cada monômero fotocurado sob diferentes atmosferas com a variação do teor de iniciador α. tamax(ar)/tamax(N2) indica a diferença de tamax do monômero fotocurado sob ar e nitrogênio, refletindo assim a magnitude do bloqueio de oxigênio de cada monômero fotocurado; quanto maior o valor, maior o efeito de bloqueio de oxigênio. Conforme observado na Figura 5, as proporções tamax(ar)/tamax(N2) do monômero TMPTA e do monômero 3EOTMPTA foram maiores quando o teor de iniciador era pequeno e diminuíram com o aumento do teor de iniciador. Isso indica que o TMPTA monomérico e o 3EOTMPTA monomérico estão sujeitos a um efeito de bloqueio de oxigênio mais significativo quando o teor de iniciador é pequeno. Quando a quantidade de EO no monômero chega a 15, a relação tamax(ar)/tamax(N2) do monômero fica próxima de 1, ou seja, há pouca diferença na relação tamax(ar)/tamax(N2) do monômero, há pouca diferença no tamax da cura por luz sob condições de ar ou nitrogênio, o que indica que o aumento da quantidade de EO no monômero é benéfico para reduzir a polimerização de bloqueio de oxigênio da cura por UV, que pode estar relacionada ao hidrogênio ativo na estrutura do EO. A estrutura semelhante ao éter na porção do EO O α-H no -O-CH2- é facilmente substituído por oxigênio e ocorrem as seguintes reações.
A relação de tmáximo(ar)/tmáximo(N2) com teores de iniciadores no processo de cura de diferentes TMPTA etoxilados.
O α-H, por um lado, pode consumir parte do oxigênio no sistema e, por outro lado, pode terminar o radical de peróxido ROO- gerado pelo radical e pelo oxigênio, reduzindo assim o consumo de radicais reativos e redirecionando a atividade de iniciação para o segmento da cadeia com atividade de iniciação, reduzindo assim o bloqueio de oxigênio do processo de fotopolimerização.
2.3 Influência da quantidade de α-H nos monômeros sobre a agregação de bloqueio de oxigênio na fotopolimerização
Para investigar a relação entre o bloqueio de oxigênio e a quantidade de α-H nos grupos monoméricos de EO, as curvas tamax-α na Figura 4 foram ajustadas linearmente a diferentes equações, e verificou-se que o maior coeficiente de correlação foi obtido pelo ajuste linear da equação lnt=a+b/α0,5. As inclinações b obtidas dos ajustes e os coeficientes de correlação R estão listados na Tabela 2.
| O valor de b e R por ajuste linear 1/α0,5 e lnt | ||||
| Monômero | ar | N2 | ||
| b | R | b | R | |
| TMPTA | 0.056 | 0.99894 | 0.0213 | 0.95494 |
| EO3TMPTA | 0.0554 | 0.95877 | 0.0257 | 0.98564 |
| 15EOTMPTA | 0.0531 | 0.96578 | 0.062 | 0.98944 |
Comparando os valores de μ correspondentes a diferentes monômeros na Figura 6, μ tem um valor máximo quando o monômero é TMPTA, ou seja, o efeito de bloqueio de oxigênio é maior quando o monômero TMPTA é curado por UV. À medida que a quantidade de EO no monômero aumenta, a quantidade de α-H no monômero aumenta e o valor de μ diminui, indicando que a barreira de oxigênio está relacionada à quantidade de α-H no monômero, que retém os radicais de oxigênio e peróxido no sistema e alivia a barreira de oxigênio. A viscosidade é uma propriedade relacionada à estrutura molecular, que envolve as propriedades de fluxo do monômero, portanto, é necessário discutir mais profundamente o efeito das propriedades de fluxo do monômero na polimerização com barreira de oxigênio.
2.4 Influência das propriedades de fluxo dos monômeros na agregação da barreira de oxigênio
As propriedades de fluxo do sistema estão relacionadas à estrutura da molécula. Em geral, quanto mais flexível for a cadeia molecular, menor será a barreira rotacional dentro da cadeia, mais curto será o segmento da cadeia como uma unidade móvel e quanto menor for a energia de ativação da cadeia molecular flexível, melhor será a mobilidade. Quanto maior o peso molecular, maior a resistência de atrito interno ao movimento molecular e menor a mobilidade [19]. Portanto, a introdução de grupos EO no monômero TMPTA alterará as propriedades de fluxo do sistema. Usando um reômetro com uma taxa de cisalhamento constante de 19,1 /min e uma taxa de aumento de temperatura de 2 °C/min, as curvas de viscosidade de cada monômero foram medidas com a temperatura. As curvas de viscosidade-temperatura de cada monômero foram ajustadas à equação de Arrhenius, e a energia de ativação de fluxo calculada E, o pré-fator A e a viscosidade do monômero η a 25 ℃ foram listados na Tabela 3.
| O valor da viscosidade η (25 ℃), a energia de ativação de fluxo E e o fator pré-exponencial A dos monômeros | |||
| Monômero | η/Pa-s(25℃) | A/10-8 | E/J |
| TMPTA | 0.01934 | 15.53 | 29079.88 |
| 3EOTMPTA | 0.06948 | 2.65 | 36600.47 |
| 15EOTMPTA | 0.18016 | 6.28 | 36821.87 |
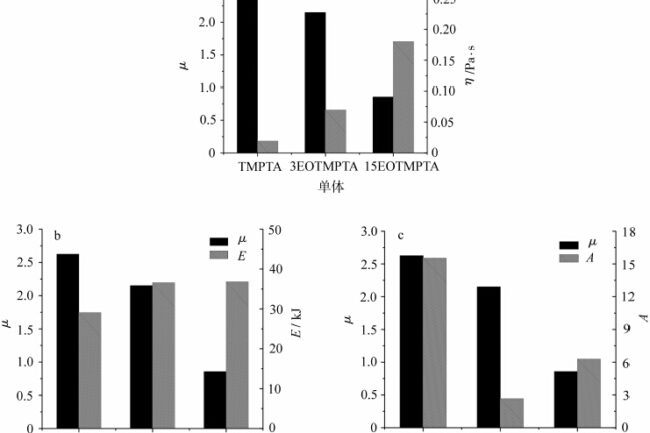
Entre eles, a energia de ativação do fluxo E está relacionada à estrutura molecular e é influenciada pela rigidez e flexibilidade da cadeia molecular, pelo tamanho e pela polaridade dos grupos laterais, etc. O fator de índice frontal A é uma constante relacionada ao peso molecular. Para investigar a relação entre as propriedades de fluxo dos monômeros e a barreira de oxigênio, os valores de μ de diferentes monômeros foram correlacionados com as viscosidades correspondentes η, a energia de ativação de fluxo E e o fator de frente de índice A, conforme mostrado na Figura 7.
A Figura 7 representa a comparação dos valores de μ de diferentes monômeros em relação à energia de ativação de fluxo E, ao fator de frente de dedo A e à viscosidade η, respectivamente. Conforme observado na Fig. 7a, o valor de μ tende a diminuir à medida que o número de EOs no monômero aumenta e a viscosidade do monômero aumenta. O tamanho da agregação de bloqueio de oxigênio está intimamente relacionado à concentração de oxigênio, e quanto maior a concentração de oxigênio, mais óbvio é o bloqueio de oxigênio [7]. No interior do sistema de fotopolimerização, a quantidade de oxigênio dissolvido é certa, e a taxa de extinção e eliminação de radicais livres pelo oxigênio no processo de fotopolimerização é extremamente rápida, e o oxigênio consumido é reabastecido principalmente pela difusão do oxigênio do ar para o interior do sistema continuamente, o que certamente envolverá a capacidade de movimentação do oxigênio no sistema, e a capacidade de movimentação do oxigênio no sistema está relacionada à viscosidade do sistema. Quando a viscosidade do sistema é baixa, o oxigênio no ar é mais fácil de se difundir para o interior do sistema, mostrando um efeito de bloqueio de oxigênio maior, de modo que o valor μ do monômero TMPTA é maior e é significativamente bloqueado pelo oxigênio. Quando a viscosidade do sistema aumenta, a capacidade de movimentação do oxigênio no sistema diminui e é tarde demais para repor o oxigênio consumido pela eliminação de radicais livres, e o bloqueio de oxigênio diminui. Como pode ser visto na figura, quando a quantidade de EO no monômero aumenta para 15, a viscosidade do monômero continua a aumentar e o valor de μ tende a 1, ou seja, a diferença entre a fotopolimerização ao ar e ao nitrogênio não é significativa.
Em seguida, compare a energia de ativação de fluxo e o fator de frente de dedo do monômero com o valor μ. Como visto na Figura 7b, a energia de ativação do fluxo do monômero aumenta de TMPTA para 3EOTMPTA com a introdução de grupos EO no monômero. Quando a quantidade de EO no monômero foi aumentada de 3 para 15, a energia de ativação do fluxo permaneceu basicamente inalterada, o que indica que o aumento da quantidade de EO no monômero basicamente não tem efeito sobre a energia de ativação do fluxo. Isso ocorre porque, embora o número de EOs no monômero aumente, o número de unidades cinemáticas não muda, o que mostra que, para o monômero TMPTA EO-ized, o efeito da energia de ativação do fluxo na barreira de oxigênio não é significativo. Conforme observado na Fig. 7c, o prefator de dedo A muda muito de TMPTA para 3EOTMPTA, o que pode estar relacionado à presença ou ausência de grupos EO. Com o aumento do número de EO no monômero, o prefator A aumenta, o que se deve ao aumento do número de EO no monômero, levando ao aumento do peso molecular do monômero. Pode-se demonstrar que, para monômeros de TMPTA EO-ized, o aumento no número de EOs na molécula leva a um aumento no peso molecular, o que leva a um aumento na viscosidade do monômero e, portanto, reduz a barreira de oxigênio. No caso de materiais poliméricos, a viscosidade do sistema geralmente pode ser aumentada com o aumento da rigidez da cadeia molecular, com o aumento da polaridade dos grupos laterais, com o aumento do peso molecular etc. Pode-se especular que os efeitos adversos do bloqueio de oxigênio da fotopolimerização podem ser reduzidos pela composição adequada da formulação, como a introdução de estruturas contendo hidrogênio ativo, o aumento da proporção de moléculas rígidas e o aumento do peso molecular.
3 Conclusão
(1) O aumento do número de grupos EO na molécula do monômero pode reduzir a agregação de bloqueio de oxigênio durante o processo de fotopolimerização. Isso está relacionado ao aprisionamento de radicais de oxigênio e peróxido pelo α-H nesse grupo e ao aumento da viscosidade do sistema.
(2) Para vários TMPTAs com OE selecionados para este estudo, a energia de ativação de fluxo do monômero tem pouco efeito sobre a agregação de bloqueio de oxigênio. O aumento na quantidade de EO no monômero leva a um aumento em seu peso molecular, o que leva a um aumento na viscosidade do monômero, que, por sua vez, afeta a agregação de barreira de oxigênio.
Monômero UV Produtos da mesma série
| Poliol/Polimercaptana | ||
| Monômero DMES | Sulfeto de bis(2-mercaptoetil) | 3570-55-6 |
| Monômero DMPT | THIOCURE DMPT | 131538-00-6 |
| Monômero de PETMP | 7575-23-7 | |
| Monômero PM839 | Polioxi(metil-1,2-etanodil) | 72244-98-5 |
| Monômero monofuncional | ||
| Monômero HEMA | Metacrilato de 2-hidroxietil | 868-77-9 |
| Monômero HPMA | Metacrilato de 2-hidroxipropila | 27813-02-1 |
| Monômero THFA | Acrilato de tetrahidrofurfurila | 2399-48-6 |
| Monômero HDCPA | Acrilato de diciclopentenila hidrogenado | 79637-74-4 |
| Monômero DCPMA | Metacrilato de di-hidrodiciclopentadienila | 30798-39-1 |
| Monômero DCPA | Acrilato de di-hidrodiciclopentadienila | 12542-30-2 |
| Monômero DCPEMA | Metacrilato de diciclopenteniloxietil | 68586-19-6 |
| Monômero DCPEOA | Acrilato de diciclopenteniloxietil | 65983-31-5 |
| Monômero NP-4EA | (4) nonilfenol etoxilado | 50974-47-5 |
| Monômero LA | Acrilato de laurila / Acrilato de dodecila | 2156-97-0 |
| Monômero THFMA | Metacrilato de tetrahidrofurfurila | 2455-24-5 |
| Monômero de PHEA | ACRILATO DE 2-FENOXIETIL | 48145-04-6 |
| Monômero LMA | Metacrilato de lauril | 142-90-5 |
| Monômero IDA | Acrilato de isodecila | 1330-61-6 |
| Monômero IBOMA | Metacrilato de isobornila | 7534-94-3 |
| Monômero IBOA | Acrilato de isobornila | 5888-33-5 |
| Monômero EOEOEA | 2-(2-Etoxietoxi)acrilato de etila | 7328-17-8 |
| Monômero multifuncional | ||
| DPHA Monômero | 29570-58-9 | |
| Monômero DI-TMPTA | TETRAACRILATO DE DI(TRIMETILOLPROPANO) | 94108-97-1 |
| Monômero de acrilamida | ||
| Monômero ACMO | 4-acriloilmorfolina | 5117-12-4 |
| Monômero di-funcional | ||
| Monômero PEGDMA | Dimetacrilato de poli(etilenoglicol) | 25852-47-5 |
| Monômero TPGDA | Diacrilato de tripropilenoglicol | 42978-66-5 |
| Monômero TEGDMA | Dimetacrilato de trietilenoglicol | 109-16-0 |
| Monômero PO2-NPGDA | Diacrilato de neopentileno glicol propoxilado | 84170-74-1 |
| Monômero de PEGDA | Diacrilato de polietileno glicol | 26570-48-9 |
| Monômero PDDA | Ftalato de diacrilato de dietilenoglicol | |
| Monômero NPGDA | Diacrilato de neopentil glicol | 2223-82-7 |
| Monômero HDDA | Diacrilato de hexametileno | 13048-33-4 |
| Monômero EO4-BPADA | DIACRILATO DE BISFENOL A ETOXILADO (4) | 64401-02-1 |
| Monômero EO10-BPADA | DIACRILATO DE BISFENOL A ETOXILADO (10) | 64401-02-1 |
| Monômero EGDMA | Dimetacrilato de etilenoglicol | 97-90-5 |
| Monômero DPGDA | Dienoato de Dipropileno Glicol | 57472-68-1 |
| Monômero Bis-GMA | Bisfenol A Metacrilato de glicidila | 1565-94-2 |
| Monômero trifuncional | ||
| Monômero TMPTMA | Trimetacrilato de trimetilolpropano | 3290-92-4 |
| Monômero de TMPTA | Triacrilato de trimetilolpropano | 15625-89-5 |
| Monômero PETA | 3524-68-3 | |
| Monômero de GPTA ( G3POTA ) | TRIACRILATO DE GLICERIL PROPOXI | 52408-84-1 |
| Monômero EO3-TMPTA | Triacrilato de trimetilolpropano etoxilado | 28961-43-5 |
| Monômero fotorresistente | ||
| Monômero IPAMA | Metacrilato de 2-isopropil-2-adamantila | 297156-50-4 |
| Monômero ECPMA | Metacrilato de 1-etilciclopentila | 266308-58-1 |
| Monômero ADAMA | Metacrilato de 1-amantílico | 16887-36-8 |
| Monômero de metacrilatos | ||
| Monômero TBAEMA | Metacrilato de 2-(terc-butilamino)etila | 3775-90-4 |
| Monômero NBMA | Metacrilato de n-butilo | 97-88-1 |
| Monômero MEMA | Metacrilato de 2-metoxietil | 6976-93-8 |
| Monômero i-BMA | Metacrilato de isobutilo | 97-86-9 |
| Monômero EHMA | Metacrilato de 2-etil-hexila | 688-84-6 |
| Monômero EGDMP | Bis(3-mercaptopropionato) de etilenoglicol | 22504-50-3 |
| Monômero EEMA | 2-etoxietil 2-metilprop-2-enoato | 2370-63-0 |
| Monômero DMAEMA | N,M-Dimetilaminoetil metacrilato | 2867-47-2 |
| Monômero DEAM | Metacrilato de dietilaminoetila | 105-16-8 |
| Monômero CHMA | Metacrilato de ciclohexila | 101-43-9 |
| Monômero BZMA | Metacrilato de benzila | 2495-37-6 |
| Monômero BDDMP | Di(3-mercaptopropionato) de 1,4-butanodiol | 92140-97-1 |
| Monômero de BDDMA | 1,4-Butanodioldimetacrilato | 2082-81-7 |
| Monômero AMA | Metacrilato de alila | 96-05-9 |
| Monômero AAEM | Metacrilato de acetilacetoxietil | 21282-97-3 |
| Monômero de acrilatos | ||
| Monômero de IBA | Acrilato de isobutilo | 106-63-8 |
| Monômero EMA | Metacrilato de etila | 97-63-2 |
| Monômero DMAEA | Acrilato de dimetilaminoetila | 2439-35-2 |
| Monômero DEAEA | 2-(dietilamino)etil prop-2-enoato | 2426-54-2 |
| Monômero CHA | ciclohexil prop-2-enoato | 3066-71-5 |
| Monômero BZA | prop-2-enoato de benzila | 2495-35-4 |