As saponinas são uma classe de glicosídeos em que os aglicones são compostos de triterpeno ou esterano. Elas são um dos ingredientes eficazes de muitos medicamentos fitoterápicos chineses, como o ginseng, o alcaçuz e o inhame (a estrutura principal das saponinas é mostrada na Figura 1). Aumentam a imunidade e outras funções. Há muitos relatórios sobre a biotransformação de ginsenosídeos na literatura. Atualmente, mais de 150 tipos de ginsenosídeos foram separados e identificados. O conteúdo dos ginsenosídeos Rb1, Rb2, Rc, Rd, Re e Rg1 chega a 80%, enquanto o conteúdo dos ginsenosídeos Rg3, Rh2, F2 e Composto K (C-K) e outras saponinas raras têm pouco ou nenhum conteúdo. Estudos demonstraram que algumas saponinas raras têm boas atividades farmacológicas. Entretanto, devido ao baixo teor, a preparação e a produção são restritas. O mesmo tipo de ginsenosídeo tem o mesmo aglicona, mas a cadeia de açúcar é diferente. Os ginsenosídeos raros e o maior teor do mesmo tipo de saponinas geralmente diferem apenas em 2 a 3 grupos de açúcar. Portanto, o mesmo tipo de saponina rara ativa pode ser preparado por hidrólise enzimática de saponina de alto teor.
Quick answer: A practical enzyme or food-ingredient decision starts with the process target, then checks activity, application window, sensory impact, and batch-to-batch consistency before scale-up.
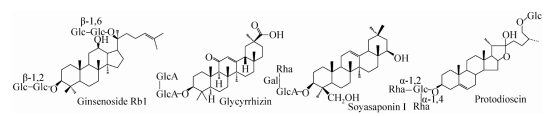
Figura 1. Estrutura das principais saponinas
Diferentes hidrolases de glicosídeos têm diferentes seletividades, e as vias para hidrolisar os ginsenosídeos também são diferentes. Conforme mostrado na Tabela 1, diferentes hidrolases de glicosídeo podem ser usadas para preparar diferentes ginsenosídeos raros. O ginsenosídeo Rd pode ser preparado pela hidrólise dos ginsenosídeos Rb1, Rb2, Rb3 e do grupo de açúcar externo C-20 de Rc. A β-glucosidase isolada e purificada do caracol de jade branco da China e do Thermus caldophilus pode converter o ginsenosídeo Rb1 em Rd. Kim et al. a obtiveram de microrganismos do solo usando a tecnologia de clonagem molecular para converter o ginsenosídeo Rb1, que é a glicosídeo hidrolase recombinante de Rd. Posteriormente, os pesquisadores clonaram a glucosidase da Thermotoga thermarum e da Bifidobacterium longum H-1, o que melhorou a eficiência da transformação e da preparação do ginsenosídeo Rd. A glucosidase obtida de Flavobacterium johnsoniae e Thermus thermophilus por meio de tecnologia recombinante pode não apenas converter o ginsenosídeo Rb1 em Rd, mas também hidrolisar a cadeia de açúcar C-20 do ginsenosídeo XVII (G17) para produzir o ginsenosídeo F2. Além da glucosidase, a α-L-arabinofuranosídeo hidrolase, que pode converter o ginsenosídeo Rc em Rd, foi obtida da raiz do ginseng e da Leuconostoc sp. A Α-L-arabinofuranosídeo hidrolase e a α-L-arabinopiranosídeo hidrolase foram obtidas da Bifidobacterium breve e da Bifidobacterium longum, que podem transformar os ginsenosídeos Rc e Rb2 em Rd. Foi relatado na literatura que a α-L-arabinofuranosídeo hidrolase em Caldicellulosiruptor saccharolyticus e Rhodanobacter ginsenosidimutans pode não apenas hidrolisar o ginsenosídeo Rc em Rd, mas também converter o composto Mc1 (C-Mc1) em F2. A hidrolase de glicosídeo isolada e purificada de Aspergillus por Yu et al. pode converter todos os ginsenosídeos Rb1, Rb2, Rb3 e Rc em Rd. Algumas hidrolases de glicosídeo podem hidrolisar completamente as cadeias de açúcar na posição C-20 em moléculas como os ginsenosídeos do tipo glicol Rb1, Rb2, Rb3, Rc e Rd, para gerar o ginsenosídeo Rg3, que permite a produção em larga escala de Rg3 e é desenvolvido como um medicamento antitumoral. A glucosidase em Paecilomyces bainier e Microbacterium esteraromaticum pode hidrolisar diretamente o ginsenosídeo Rb1 em Rg3, enquanto a glucosidase isolada e purificada de Microbacterium esteraromaticum pode hidrolisar o ginsenosídeo Rb2 em Rg3. A hidrolase de glicosídeo recombinante clonada da Pseudonocardia pela tecnologia de clonagem molecular pode transformar os ginsenosídeos Rb1, Rb3 e Rd para preparar o Rg3. Da mesma forma, uma série de ginsenosídeos raros ativos pode ser preparada pela hidrólise do grupo de açúcar na posição C-3 dos ginsenosídeos. A glucosidase recombinante clonada de Sphingomonas e Sphingopyxis alaskensis pode hidrolisar a glicose fora da cadeia de açúcar na posição C-3 nas moléculas de ginsenosídeo Rb1, Rb2, Rc, Rd e Rg3 e preparar G17, Composto O (CO) e C-Mc1, F2 e Rh2. Algumas glicosidases podem hidrolisar diretamente o grupo glucosil interno na posição C-3. Por exemplo, a glucosidase de Terrabacter ginsenosidimutans e Esteya vermicola pode hidrolisar a cadeia de açúcar na posição C-3 das moléculas de ginsenosídeo Rb1, Rb2, Rb3, Rc e Rd para produzir a saponina correspondente LXXV (G75), o Composto Y (C-Y), o Composto Mx (C-Mx), o Composto Mc (C-Mc) e C-K. Além disso, algumas hidrolases de glicosídeo podem hidrolisar simultaneamente os grupos de açúcar C-20 e C-3 em ginsenosídeos do tipo glicol. A glucosidase recombinante clonada de Arthrobacter chlorophenolicus pode converter os ginsenosídeos Rb1, Rb2 e Rc em F2. A hidrolase de glicosídeo da Fusobacterium K60, os fungos endofíticos GE 17-18, Sulfolobus acidocaldarius, Aspergillus niger e Microbacteriu esteraromaticum podem hidrolisar o ginsenosídeo Rb1 para produzir C-K.
Tabela 1. Biotransformação de ginsenosídeos por glicosidase
| Produto | Substrato | Reação | Organismo |
| Rd | Rb1 | β-Glucosidase | Caracol de jade branco da China |
| Rd | Rb1 | β-Glucosidase | Thermus caldofilo |
| Rd | Rb1 | β-Glucosidase | Bactérias não cultivadas |
| Rd | Rb1 | β-Glucosidase | Thermotoga termal |
| Rd | Rb1 | β-Glucosidase | Bifidobacterium longum H-1 |
| Rd | Rb1 | β-Glucosidase | Flavobactéria johnsoniae |
| Rd | Rb1 | β-Glucosidase | Thermus termófilo |
| Rd | Rb1 | β-Glucosidase | Penicillium oxalicum |
| Rd | Rb1 | β-Glucosidase | Cladosporium fulvo |
| Rd | Rc | α-L-Arabinofuranosidase | Panax ginseng |
| Rd | Rc | α-L-Arabinofuranosidase | Leuconostoc |
| Rd | Rc | α-L-Arabinofuranosidase | Bifidobacterium breve |
| Rd | Rc | α-L-Arabinofuranosidase | Bifidobacterium longum |
| Rd | Rc | α-L-Arabinofuranosidase | Caldicellulosiruptor saccharolyticus |
| Rd | Rc | α-L-Arabinofuranosidase | Rhodanobacter ginsenosidimutans |
| Rd | Rb2 | α-L-Arabinopiranosidase | Bifidobacterium breve |
| Rd | Rb2 | α-L-Arabinopiranosidase | Bifidobacterium longum |
| Rd | Rb1/Rb2/Rb3/Rc | Glicosidase | Aspergillus |
| Rg3 | Rb1 | β-Glucosidase | Paecilomyces bainier |
| Rg3 | Rb1 | β-Glucosidase | Microbactéria esteraromático |
| Rg3 | Rb2 | β-Glucosidase | Microbactéria esteraromático |
| Rg3 | Rb1/Rb3/Rd | β-Glucosidase | Pseudonocardia |
| G17 | Rb1 | β-Glucosidase | Sphingomonas |
| G17 | Rb1 | β-Glucosidase | Esfingopixe alaskensis |
| G17 | Rb1 | β-Glucosidase | Cellulosimicrobium celulanos |
| G75 | Rb1 | β-Glucosidase | Terrabacter ginsenosidimutans |
| G75 | Rb1 | β-Glucosidase | Esteya vermicola |
| F2 | G17 | β-Glucosidase | Flavobactéria johnsoniae |
| F2 | G17 | β-Glucosidase | Thermus termófilo |
| F2 | C-Mc1 | α-L-Arabinofuranosidase | Caldicellulosiruptor saccharolyticus |
| F2 | C-Mc1 | α-L-Arabinofuranosidase | Rhodanobacter ginsenosidimutans |
| F2 | Rd | β-Glucosidase | Cellulosimicrobium celulanos |
| F2 | Rb1/Rb2/Rc | β-Glucosidase | Arthrobacter clorofenólico |
| Rh2 | Rg3 | β-Glucosidase | Esfingopixe alaskensis |
| CK | Rd | β-Glucosidase | Terrabacter ginsenosidimutans |
| CK | Rd | β-Glucosidase | Esteya vermicola |
| CK | Rb1 | β-Glucosidase | Fusobactéria K-60 |
| CK | Rb1 | β-Glucosidase | fungos endofíticos GE 17-18 |
| CK | Rb1/Rb2 | β-Glucosidase | Sulfolobus acidocaldário |
| CK | Rb1/Rb2/Rb3/Rc | β-Glucosidase | Aspergillus Níger |
| CK | Rb1/Rb2 | β-Glucosidase | Microbactérias esteraromático |
| C-O | Rb2 | β-Glucosidase | Cellulosimicrobium celulanos |
| C-Y | Rb2 | β-Glucosidase | Terrabacter ginsenosidimutans |
| C-Mc | Rc | β-Glucosidase | Terrabacter ginsenosidimutans |
| C-Mc1 | Rc | β-Glucosidase | Cellulosimicrobium cellulans |
| C-Mx | Rb3 | β-Glucosidase | Terrabacter ginsenosidimutans |
| Rg2 | Re | β-Glucosidase | Microbacterium esteraromaticum |
| Rg2 | Re | β-Glucosidase | Mucilaginibacter |
| Rg2 | Re | β-Glucosidase | Pseudonocardia |
| Rh1 | Rg1 | β-Glucosidase | Microbacterium esteraromaticum |
| Rh1 | Rf | β-Glucosidase | Pyrococcus furiosus |
| Rh1 | Rf | β-Glucosidase | Aspergillus niger |
| Rh1 | Rg2 | α-L-Rhamnosidase | Absidia |
| Rh1 | R2 | β-xilosidase | Thermoanaerobacterium |
| F1 | Rg1 | β-Glucosidase | Fusarium moniliforme |
| F1 | Rg1 | β-Glucosidase | Penicillium sclerotiorum |
| F1 | Rg1 | β-Glucosidase | Sanguibacter keddieii |
G17: gypenoside XVII; G75: gypenoside LXXV; C-O: composto O; C-Y: composto Y; C-Mc1: composto Mc1; C-Mc: composto Mc; C-Mx: composto Mx; C-K: composto K.
Os grupos de açúcar C-6 e C-20 nos ginsenosídeos triol também podem ser hidrolisados por hidrolases de glicosídeo. O ginsenosídeo Rg2 pode ser obtido pela hidrólise da glicose C-20 na molécula de Re pela glicosidase. A glucosidase recombinante clonada de Microbacterium esteraromaticum, Mucillaginibacter e Pseudonocardia pode não apenas converter o ginsenosídeo Re em Rg2, mas também o ginsenosídeo Rg1 é convertido em Rh1. A glicose, a ramnose e a xilose fora da posição C-6 do ginsenosídeo Rf, Rg2 e R2 podem ser convertidas para preparar Rh1. Ao contrário do ginsenosídeo Rh1, o ginsenosídeo F1 tem apenas uma glicose ligada à posição C-20 de seu aglicona. A glucosidase em Fusarium moniliforme, Penicillium sclerotiorum e Sanguibacter keddieii pode hidrolisar especificamente a glicose C-6 do ginsenosídeo Rg1 para produzir o ginsenosídeo F1.
A glicosídeo hidrolase não é usada apenas para transformar e preparar ginsenosídeos raros ativos, mas também é amplamente usada para hidrolisar e modificar saponinas como as do alcaçuz, da soja e do inhame (Tabela 2). A glucuronidase isolada e purificada de Streptococcus LJ-22 e Penicillium purpurogenum Li-3 pode hidrolisar a glicirrizina para produzir ácido monoglucurônico de glicirrizina, e não há subproduto ácido glicirretínico. Morana et al. usaram a glucuronidase derivada do Aspergillus niger para hidrolisar completamente a glicirrizina e produzir o ácido glicirretínico. A hidrolase de sojaaponina isolada e purificada de Aspergillus oryzae pode hidrolisar a sojaaponina I para produzir sojaaponol B. Uma nova hidrolase de saponina de soja em Neocosmospora vasinfecta pode converter a saponina de soja I, II e III em saponina de soja B, o que proporciona uma ferramenta eficaz para a preparação de saponina de soja com regulação antioxidante e de lipídios no sangue. Entre as saponinas esteroidais, a pesquisa e a comparação da modificação da hidrólise da cadeia de açúcar da dioscina são sistemáticas. Inoue et al. isolaram e purificaram uma glucosidase de Costus speciosus que pode hidrolisar a diosgenina original para produzir diosgenina. Liu et al. isolaram, purificaram e clonaram de Aspergillus oryzae para obter uma hidrolase de dioscina recombinante, que pode hidrolisar os grupos glucosil e α-1,4 ramnosil na dioscina para produzir dioscina III. A α-L-ramnosidase isolada e purificada por Feng et al. de Curvularia lunata pode hidrolisar o grupo α-1,2 ramnosil na dioscina para produzir dioscina V. Qian et al. isolaram e purificaram uma α-L-ramnosidase de fígado bovino fresco, que pode hidrolisar os dois grupos α-1,2 e α-1,4 ramnosil na diosgenina para formar um grupo glicose. -Diosgenina. Fu et al. isolaram e purificaram a diosgenina hidrolase da Absidia, que pode hidrolisar completamente a diosgenina em diosgenina.
Tabela 2. Biotransformação de outras saponinas por glicosidase
| Produto | Substrato | Reação | Organismo |
| GAMG | Glycyrrhizin | β-Glucuronidase | Streptococcus |
| GAMG | Glycyrrhizin | β-Glucuronidase | Penicillium purpurogenum |
| Ácido glicirretínico | Glycyrrhizin | β-Glucuronidase | Aspergillus niger |
| Sojaapogenol B | Sojasaponina I | Saponina hidrolase de soja | Aspergillus oryzae |
| Sojaapogenol B | Sojasaponina | Saponina hidrolase de soja | Neocosmospora vasinfecta |
| Dioscina | Protodioscina | β-Glucosidase | Costus speciosus |
| Progenina III | Protodioscina | Protodioscina-glicosidase | Aspergillus oryzae |
| Progenina V | Dioscina | α-L-Rhamnosidase | Curvularia lunata |
| Diosgenil-glucosídeo | Dioscina | α-L-Rhamnosidase | Fígado bovino |
| Diosgenina | Dioscina | Dioscina-glicosidase | Absidia |
GAMG: Mono-glucuronídeo do ácido glicirrético
A practical sourcing checklist for enzyme, biotech, and food-ingredient topics
In enzyme and food-processing projects, the most useful decision frame is usually application fit plus process stability: which ingredient performs under the intended pH, temperature, time, and substrate conditions without creating a downstream quality or compliance problem.
- Define the processing target first: flavor, hydrolysis, texture, fermentation, cleaning, and bioprocess applications often need very different activity profiles.
- Check the real operating window: pH, temperature, residence time, and substrate type often matter more than a headline product claim.
- Review consistency and downstream impact: dosage, sensory influence, filtration, and shelf-life behavior can all affect the final commercial value.
- Use pilot validation: small production tests usually reveal the most useful differences in activity, efficiency, and process fit.
Recommended product references
- Longzyme Lipase: A direct product reference for lipase-related food, cleaning, or bioprocess discussions.
- Longzyme Beta-Amylase: A practical enzyme reference when starch conversion and food-processing activity are under review.
- Longzyme Compound Glucoamylase: A useful enzyme reference when saccharification or related processing performance matters.
- Extrato de levedura: A practical ingredient reference when flavor, fermentation, or nutrient-support applications are involved.
FAQ for buyers and formulators
Why is a high-activity enzyme not automatically the best commercial choice?
Because the best enzyme is the one that performs reliably under the actual process conditions and gives the desired downstream result without creating new issues.
Should food and biotech ingredients be selected from data sheets alone?
It is usually safer to pair the specification review with a pilot or application test because real substrates and process windows can change the result a lot.
Entre em contato conosco agora!
Se precisar do Price, preencha suas informações de contato no formulário abaixo. Normalmente, entraremos em contato dentro de 24 horas. Você também pode me enviar um e-mail info@longchangchemical.com durante o horário comercial (das 8h30 às 18h UTC+8 de segunda a sábado) ou use o bate-papo ao vivo do site para obter uma resposta imediata.
| Composto Glucoamilase | 9032-08-0 |
| Pullulanase | 9075-68-7 |
| Xilanase | 37278-89-0 |
| Celulase | 9012-54-8 |
| Naringinase | 9068-31-9 |
| β-Amilase | 9000-91-3 |
| Glucose oxidase | 9001-37-0 |
| alfa-Amilase | 9000-90-2 |
| Pectinase | 9032-75-1 |
| Peroxidase | 9003-99-0 |
| Lipase | 9001-62-1 |
| Catalase | 9001-05-2 |
| TANNASE | 9025-71-2 |
| Elastase | 39445-21-1 |
| Urease | 9002-13-5 |
| DEXTRANASE | 9025-70-1 |
| L-Láctico desidrogenase | 9001-60-9 |
| Malato desidrogenase | 9001-64-3 |
| Colesterol oxidase | 9028-76-6 |
