Quick answer: In most UV systems, photoinitiators are selected by balancing wavelength fit, through-cure, color control, and line speed. Buyers usually compare a blended package instead of one isolated product.
PVC는 오늘날 시장에서 가장 널리 사용되는 폴리머 중 하나이며 건축 자재 및 전자 포장 분야에서 중요한 역할을 합니다. 그러나 열, 산소, 빛, 힘 등 외부 요인 (예 : 열, 산소, 빛 및 힘 등)의 PVC는 분해 및 가교 반응의 작용으로 PVC 제품이 변색되고 기계적 특성이 약화되며 110 ℃로 가열 된 PVC는 HCl 가스를 방출하여 PVC가 분해되기 시작합니다. 현재 PVC 열 안정제는 주로 납염 열 안정제, 금속 비누 열 안정제, 유기 주석 열 안정제, 유기 열 안정제 및 희토류 열 안정제의 다섯 가지 종류입니다. 납염 열 안정제는 중금속이 함유되어 있어 환경 오염이 심각하기 때문에 현재는 거의 사용되지 않습니다. 금속 비누 형 열 안정제는 처음에는 변색 방지 능력이 떨어지고 불안정한 염소 원자 치환 능력의 PVC 분해가 열악하여 시장 수요를 충족시키지 못합니다. 유기 주석 열 안정제는 상당한 안정화 효과가 있지만 일부는 독성이 있고 비용이 많이 들기 때문에 개발이 제한됩니다. 유기 열 안정제는 무독성이며 환경 친화적이지만 PVC 열 안정제만으로는 안정성이 떨어집니다. 희토류 열 안정제는 독성이 낮고 환경 보호 및 열 안정성이 우수하다는 장점이 있는 희토류 열 안정제가 더 많이 연구되었습니다.
과학 기술의 발전과 혁신으로 환경 보호는 열 안정제의 중요한 기준이 되었기 때문에 질소 함유 헤테로 사이 클릭 카르 복실 산 열 안정제가 널리 주목을 받고 있습니다. 이는 열 안정제 조성물에 중금속이 포함되어 있지 않아 오염 문제를 해결하고 열 안정성이 우수한 리간드이기 때문입니다. 질소 함유 헤테로 사이 클릭 카르 복실 산 열 안정제를 희토류 염 용액과 결합하여 새로운 유형의 질소 함유 헤테로 사이 클릭 카르 복실 산 희토류 열 안정제를 합성 할 수 있습니다. 그 장점은 낮은 독성, 환경 보호, 우수한 광 투과율, 우수한 열 안정성, 저비용, 높은 수율 및 높은 개발 잠재력입니다. 류 자오강 외. 는 이미다졸 ⁃ 4,5 ⁃ 디 카르 복실 산, 수산화 나트륨, 염화 란탄을 원료로 사용하여 질소 함유 헤테로 사이 클릭 카르 복실 산 희토류 열 안정제를 제조 한 다음 정적 열 안정화 실험과 동적 열 안정화 실험을 사용하여 추가 연구를 수행했으며 준비 과정이 비교적 번거롭고 반응 시간이 상대적으로 길지만 복합체의 열 안정성 생성물은 여전히 양호하다는 것을 발견했습니다. 장 닝 등은 아미노산, 수산화 나트륨 및 질산 란탄을 원료로 8 종류의 란탄 아미노산 열 안정제를 합성하고 정적 열 안정화 실험과 동적 열 안정화 실험을 통해 추가로 연구하고 8 종류의 란탄 아미노산의 열 안정성을 비교했습니다, 그리고 8 종류의 란탄 아미노산에는 유독하고 환경 친화적이지 않은 벤젠 고리와 황이 포함되어 있으며 8 종류의 아미노산 원료 중 트립토판에는 벤젠 고리가 포함되어 있지만 란탄 트립토판의 열 안정성이 8 종류의 아미노산보다 우수하고 란탄 트립토판의 열 안정성이 8 종류의 아미노산보다 우수하다는 것을 발견했습니다. 그러나 란탄 트립토판의 열 안정성은 8 종류의 란탄 아미노산 중에서 가장 우수하며, 복합 열 안정제의 활성화 에너지는 란탄 트립토판 모노머 및 시판되는 칼슘 및 아연 열 안정제보다 우수하여 PVC의 열 안정성을 향상시킬 수 있습니다.
본 논문에서는 열안정성 연구를 위해 2,3⁃PDA를 란탄 원소의 리간드로서 pH=6~7에서 합성하고, 2,3⁃LPDA를 PVC의 주 열안정제로 사용한 후 스테아린산 칼슘, 스테아린산 아연, 펜타에리스리톨 등과 같은 보조 열안정제와 배합하여 열안정화 효과를 비교 분석하였다, 합성된 시스템의 열 안정성을 2,3⁃LPDA의 열 안정성과 비교 분석하고, 일부 열 안정제가 PVC의 가소화 및 기계적 특성에 미치는 영향을 특성화하여 최종적으로 2,3⁃LPDA의 열 안정화 메커니즘을 규명하였습니다.
1
샘플 준비
2,3⁃LPDA 준비: 적정량의 산화 란타늄을 비커에 계량하고 탈 이온수를 넣고 잘 저어주고, 비커를 60 ℃ 수조 가열에 넣고 교반기로 산화 란타늄 수용액을 저어 준 다음 점 적기를 사용하여 질산 용액을 천천히 첨가하여 산화 란타늄 용액이 완전히 용해됩니다; 용액의 pH 값은 여과 용 pH 종이, 질산 란탄 용액에 대해 얻은 여과 액에 의해 3 ~ 4로 결정되었고, 여분의 시약 병에 부어 몰 값은 0이었고, 그 몰 값은 0이었다.015 mg/L. 용액을 여과 한 다음 시약 병에 부었습니다. 시약 병 여분, EDTA 적정으로 결정된 몰 농도, 몰 비율 3의 무게 측정:2 2,3 ⁃ PDA와 질산 란탄산염, 첫 번째 무수 에탄올은 2,3 ⁃ PDA 분말이 용해 된 다음 암모니아를 희석하여 pH를 6 ~ 7로 조정합니다, 질산 란탄 용액을 일정하게 교반하면서 2,3 ⁃ PDA의 무수 에탄올 용액에 천천히 첨가 한 다음 암모니아를 희석하여 시스템의 pH를 6 ~ 7로 조정하여 전기 교반기로 흰색 침전물을 생성합니다. 백색 침전물을 전기 교반기로 3 시간 동안 교반하여 시스템을 완전히 반응시킨 다음 침전물이 모두 침전되도록 방치 한 다음 여과 한 다음 침전물을 무수 에탄올로 여러 번 세척하고 복합물을 50 ℃에서 일정한 무게로 건조시키고 결과물은 2,3 ⁃ LPDA 희토류 열 안정제였으며 제품을 분말로 분쇄 한 다음 예비 사용을 위해 가방에 포장했습니다;
복합 열 안정제 준비 : 2,3 ⁃ 스테아린산 아연 및 펜타 에리스리톨을 함유 한 LPDA와 2 진 및 3 진 화합물의 다양한 질량 비율에 따라 분말의 무게, 분쇄 및 혼합, 예비 백 포장.
2
결과 및 토론
2.1 2,3⁃LPDA의 특성 분석
2.1.1 적외선 스펙트럼 분석
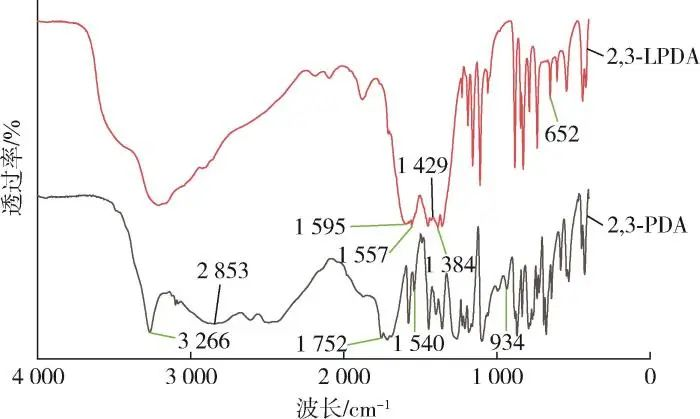
그림 1은 2,3⁃PDA와 2,3⁃LPDA의 FTIR 스펙트럼을 보여줍니다. 2,3⁃PDA와 2,3⁃LPDA에서 C=N 결합의 텔레스코픽 진동 피크는 각각 1,540 cm-1과 1,557 cm-1에서, 2,3⁃LPDA에서 NO3-의 텔레스코픽 진동 피크는 1,384 cm-1에서 나타나는 것을 볼 수 있습니다; 2,3⁃PDA에서 C=O 결합의 텔레스코픽 진동 피크 1,752 cm-1; 2,3⁃PDA에서 C=O 결합의 텔레스코픽 진동 피크 각각 1,595 cm-1 및 1,429 cm-1; 2,3⁃PDA의 텔레스코픽 진동 피크 각각 1,595 cm-1 및 1,429 cm-1에서 2,3 ⁃PDA의. 1,595 cm-1과 1,429 cm-1에서 각각 2,3⁃LPDA의 C=O 결합의 비대칭 및 대칭 텔레스코픽 진동 피크, 3,266 cm-1은 2,3⁃PDA의 O-H 결합의 텔레스코픽 진동 피크, 934 cm-1은 카복실레이트기가 존재함을 확인할 수 있는 특징적으로 넓은 피크인 -COOH의 2,3⁃PDA에서 나타나는 특징적인 피크를 확인할 수 있습니다; 2,3⁃LPDA에서 O-La 결합의 연신 진동 피크는 652 cm-1로, 2,3⁃PDA와 질산 란탄이 리간드로 반응하여 2,3⁃PDA의 카르복실 레이트기의 O-H 결합이 사슬을 끊고 de-H를 생성하여 La 이온과 O-La 결합을 형성했음을 나타냅니다. 요약하면, 이 반응으로 2,3⁃LPDA가 생성되었다는 것을 알 수 있습니다.
그림 1 샘플의 FTIR 스펙트럼
2.1.2 원소 및 열 분석
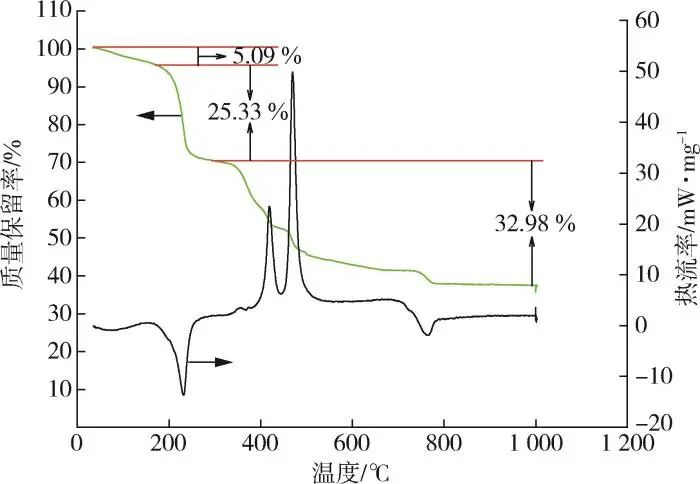
2,3⁃LPDA에서 C, H 및 N의 원소 함량은 원소 분석에 의해 결정되었고 란탄 함량은 EDTA 적정법에 의해 결정되었습니다. 표 1을 통해 원소 H 함량 (질량 분율, 이하 동일)의 상대적 오차는 소량으로 인해 크며 다른 원소의 실제 함량은 기본적으로 이론적 함량과 일치 함을 알 수 있습니다. 그런 다음 그림 2의 열 분석 결과에 의해 결정화 물의 수를 계산하여 2,3⁃LPDA의 분자식을 La2 (C6N2O4) 2 (NO3) 2-3H2O로 유도했습니다. 그림 2의 TG 곡선에서 2,3⁃LPDA의 열 중량 손실은 각각 50에서 184, 184에서 292, 292에서 1,000 ℃의 3 단계로 나뉘는 것을 알 수 있습니다. 첫 번째 단계의 질량 손실률은 5.09 %였으며, 질량 손실률로부터 결정수가 3 개가 있음을 추론했습니다.표 1에서 추론한 분자식 La2(C6N2O4)2(NO3)2-3H2O의 결정수 함량은 88 %이며, 1단계의 DSC 곡선은 87.1~140.6℃에서 열흡수 피크가 발생하여 2,3 ⁃LPDA에서 결정수가 제거된 것을 나타냈습니다. 2단계와 3단계의 TG 곡선에서 2,3 ⁃LPDA는 2단계와 3단계에서 총 질량 손실이 58.31%로 급격한 중량 감소를 보였으며, DSC 곡선과 달리 2단계에서 제품의 분해를 나타내는 184~292.4℃의 흡광 피크가 나타났습니다. 세 번째 단계에서는 제품의 추가 분해를 나타내는 두 개의 발열 피크가 나타났습니다. 797 ℃ 이후에는 더 이상 무게 감소가 없었고 TG 곡선은 평평 해지는 경향이 있으며 최종 잔류 물은 질량 분율의 36.59%를 차지하는 La2O3이며 La의 함량은 표 1의 이론적 인 La 함량 31.53%와 유사한 31.11%로 계산됩니다. 요약하면, 표 1과 그림 2의 데이터를 비교하여 희토류 열 안정제의 분자식은 La2(C6N2O4)2(NO3)2-3H2O로 결정되었습니다.
표 1 2,3⁃LPDA의 원소 분석 결과
그림 2 2,3⁃LPDA의 열 분석 곡선
2.2 열 안정성 분석
2.2.1 단일 열 안정제
2,3⁃LPDA의 열 안정성을 더 깊이 연구하기 위해 일반적인 열 안정제와 열 안정성을 각각 비교했으며 그 결과는 표 2에 나와 있습니다. 표 2에 따르면 2,3⁃LPDA의 열 안정화 시간은 30 분으로 2,3⁃PDA보다 6 배 더 길고 스테아린산 납보다 짧고 표에있는 다른 열 안정제보다 길다는 것을 알 수 있습니다. 변색 방지 성능 측면에서 2,3⁃LPDA는 2,3⁃PDA보다 초기 변색 방지 성능이 더 우수하며, 이는 2,3⁃LPDA가 불안정한 Cl-와의 결합 능력이 더 강하고 PVC의 초기 변색 방지 성능을 향상 시킨다는 것을 나타냅니다. 장기 변색 방지 성능 측면에서 2,3⁃LPDA는 변색 방지 능력이 칼슘 스테아 레이트 및 펜타 에리스리톨보다 약간 약합니다. 스테아린산 칼슘과 펜타에리스리톨을 제외하고 2,3⁃LPDA는 변색 방지 성능에서 다른 열 안정제에 비해 몇 가지 장점이 있으며 PVC의 열 저하를 방지하는 데 긍정적 인 영향을 미칩니다.
표 2 다양한 열 안정제의 열 안정성
2.2.2 스테아린산 아연과 합성된 2,3⁃LPDA
2,3⁃LPDA의 초기 변색 저항성은 스테아린산 아연보다 약간 떨어지지만 열 안정화 시간과 장기 변색 저항성은 스테아린산 아연보다 훨씬 우수합니다. 두 복합체의 열 안정성 테스트 결과는 표 3에 나와 있습니다. 표 3에서 2,3⁃LPDA와 스테아린산아연의 배합비를 4:1로 했을 때 열안정 시간이 34분으로 가장 길었고, 2,3⁃LPDA를 단독으로 열안정제로 사용했을 때보다 길었으며 배합비에서 2,3⁃LPDA의 비율이 커질수록 열안정 시간이 길다는 것을 알 수 있습니다. 이는 Re3+와 Cl-가 강한 배위 효과를 가지고 있어 열에 의해 분해되는 Cl-와 더 쉽게 배위되기 때문입니다. 변색 방지 성능 측면에서, 복합 열 안정제의 초기 변색 방지 성능이 크게 향상되었습니다. 이는 아연 스테아레이트의 2,3 ⁃ LPDA 초기 억제가 "아연 연소"현상을 생성하는 것이 분명하고 강력한 시너지 효과가 있으며 PVC의 초기 변색 방지 성능의 복합화가 크게 향상되었기 때문입니다. 그러나 장기 변색 방지 성능에서 2,3 ⁃ LPDA 단독은 복합 변색 방지 성능보다 우수하고 2,3 ⁃ LPDA는 더 작은 비율의 배합 비율에서 "아연 연소" 현상이 더 분명할수록 장기 변색 방지가 더 나빠질 것입니다, 열 안정화 시간이 짧아져 배합 비율에서 스테아르 산 아연의 비율이 많을수록 2,3 ⁃ LPDA와 스테아르 산 아연의 비율이 많고 2,3 ⁃ LPDA와 스테아르 산 아연의 비율이 많을수록 2,3 ⁃ LPDA와 아연의 비율이 많을수록 열 안정화 시간이 짧아짐을 나타냅니다. 열 안정화 시간이 짧을수록 배합 비율에서 스테아린산 아연의 비율이 높을수록 LPDA와 스테아린산 아연 간의 시너지 효과가 떨어짐을 나타냅니다.
표 3 스테아린산 아연 복합 시스템의 열 안정성
2.2.3 펜타에리스리톨과 2,3⁃LPDA의 복합화
펜타에리스리톨은 열 안정성이 우수한 보조 열 안정제이며 장단기 변색 방지 성능이 우수합니다. 2,3⁃LPDA와 펜타에리스리톨이 복합된 열 안정성은 표 4에 나와 있습니다. 표에서 두 가지 복합 열 안정제의 열 안정 시간은 31-34 분 범위이며, 열 안정제로서 2,3 ⁃LPDA 단독의 열 안정 시간은 30 분임을 알 수 있습니다, 이는 스테아린산아연과 복합된 펜타에리스리톨과 2,3⁃LPDA의 열안정 시간이 30분으로 2,3⁃LPDA와 스테아린산아연의 시너지 효과가 점점 더 중요하다는 것을 나타낸다고 볼 수 있습니다. 3⁃LPDA와 펜타 에리스리톨 복합 열 안정화 효과는 분명하지 않으며 열 안정화 시간은 1-3 분만 연장되지만 특정 시너지 효과도 있습니다. 변색 방지 성능 측면에서 펜타 에리스리톨의 효과는 매우 분명하며 두 복합체의 초기 변색 방지 성능은 열 안정제로서 2,3⁃LPDA 단독의 변색 방지 성능보다 우수합니다. 장기 변색 방지 성능에서 복합 열 안정제에서 펜타에리스리톨의 비율이 클수록 장기 변색 방지 능력이 향상되어 펜타에리스리톨과 2,3⁃LPDA의 복합이 우수한 변색 방지 성능을 가지며 펜타에리스리톨은 2,3⁃LPDA의 장기 변색 방지 성능을 더욱 증가 시킨다는 것을 나타냅니다. 전반적으로 펜타에리스리톨의 열 안정화 효과는 분명하지 않지만 변색 방지 특성은 매우 두드러집니다. 이는 알코올이 가열되면 PVC의 착색을 변화시키는 능력과 온도가 상승함에 따라 알코올이 에스테르 화되어 알코올이 PVC에서 침전되는 것을 더 어렵게 만들기 때문입니다. 동시에 펜타에리스리톨과 란탄은 PVC가 분해되는 동안 분자 사슬의 끊어진 사슬을 보완하기 위해 복합화되어 PVC의 장기적인 변색 방지 능력을 향상시킬 수 있습니다.
표 4 펜타에리스리톨 복합 시스템의 열 안정성
2.2.4 2,3⁃LPDA, 스테아린산아연 및 펜타에리스리톨의 배합
스테아린산 아연으로 인한 "아연 화상" 현상은 펜타에리스리톨에 의해 지연될 수 있습니다. 열 안정제의 변색 방지 능력과 열 안정화 시간을 더 우수하게 만들기 위해 2,3⁃LPDA, 스테아린산 아연 및 펜타에리스리톨을 배합했으며 그 열 안정성은 표 5에 나와 있습니다. 표 5에서 볼 수 있듯이 2,3⁃LPDA:징크스테아레이트:펜타에리스리톨의 비율이 2:1:2일 때 열 안정화 시간이 44분으로 다른 두 가지 배합 비율보다 높아 2,3⁃LPDA와 펜타에리스리톨이 같은 비율을 차지할 때 강력한 시너지 효과가 있음을 충분히 증명했습니다. 변색 방지 성능의 관점에서 볼 때 펜타 에리스리톨의 첨가로 인해 복합 시스템의 변색 방지 성능이 크게 향상되었으며 펜타 에리스리톨은 또한 스테아르 산 아연 "아연 화상"현상의 발생을 늦추고 세 가지 복합 후 시스템의 장기 변색 방지 성능이 크게 향상되었습니다. 표 2, 표 3 및 표 5를 비교하면 삼원 화합물 시스템의 변색 방지 성능이 이진 화합물보다 크게 향상되었음을 알 수 있습니다. 이는 폴리올의 보조 열 안정제가 어느 정도 스테아르 산 아연 "아연 연소"현상의 발생을 방지 할 수 있고 펜타 에리스리톨과 스테아르 산 아연의 반응에 의해 생성 된 복합체가 PVC의 분해에 대한 ZnCl2의 촉매 효과를 효과적으로 약화시킬 수 있기 때문입니다.
표 5 삼원 배합 시스템의 열 안정성
2.3 가소화 특성 분석
본 연구에서는 열안정제가 PVC의 동적 열 안정성에 미치는 영향을 연구하기 위해 다양한 열안정제에 대해 가소화 실험을 수행했으며 그 결과는 표 6에 나와 있습니다. 표에서 볼 수 있듯이 2,3⁃LPDA와 혼합된 스테아린산아연을 함유한 열안정제 샘플의 가소화 시간이 가장 길었습니다. 이는 아연 스테아 레이트 단독 가소 화, 가소 화 성능이 매우 열악하고 충전이 끝나면 즉시 "아연 연소"현상이 나타나고 현상이 PVC의 분해를 촉진하고 가소 화를 실현할 수 없으며 2,3 ⁃ LPDA 복합체를 사용하면 2,3 ⁃ LPDA가 "아연 연소"현상, "아연 연소"현상의 효과, "아연 연소"현상의 효과를 늦추는 역할을했기 때문입니다. "가소 화 피크 후 스테아린산 아연은 PVC의 분해를 촉진하기 시작하여 PVC 분말의 분해를 가속화했습니다. 삼원 열 안정제를 함유 한 샘플의 가소 화 시간은 2,3 ⁃LPDA를 함유 한 샘플보다 약간 길지만 가소 화 토크와 평형 토크가 낮아 공정 중에 PVC와 가공 기계 사이의 접착력을 줄여 에너지 손실과 전력 소비를 줄일 수 있음을 나타냅니다.
표 6 다양한 시료의 가소화 특성
2.4 인장 특성 분석
정적 열안정화 실험 결과에 따라 각 실험군에서 가장 우수한 열안정화 성능을 보인 희토류 열안정제를 인장 특성 시험에 선정하여 다양한 열안정제가 PVC의 인장 특성에 미치는 영향을 연구했으며 그 결과는 표 7에 나와 있습니다. 결과는 표 7에 나와 있습니다. 표에서 PVC에 2,3⁃LPDA를 첨가한 후 PVC의 인장 특성이 크게 향상되었음을 알 수 있습니다; 2,3⁃LPDA와 스테아린산 아연을 함유한 열안정제 샘플과 2,3 ⁃LPDA를 함유한 샘플의 인장 특성의 차이가 큰데, 이는 PVC 시트 혼합 시 일부 스테아린산 아연이 PVC의 열화를 촉진하는 "아연 탄" 현상을 보였기 때문일 수 있습니다. 이는 PVC 플레이크를 혼합하는 동안 일부 스테아린산 아연의 "아연 연소" 현상으로 인해 PVC의 열화를 촉진하고 PVC 플레이크의 인장 강도를 감소시켜 PVC 플레이크의 기계적 특성이 저하되기 때문일 수 있습니다. 표 7의 마지막 데이터는 2,3⁃LPDA, 스테아린산 아연 및 펜타에리스리톨이 PVC 인장 강도 향상에 가장 큰 영향을 미친다는 것을 보여줍니다. 이는 희토류 원소가 리간드의 외전자를 받아들이는 빈 궤도가 많고 희토류 금속 이온은 이온 반경이 커서 PVC 공식의 유기 및 무기 물질과 다양한 리간드 또는 킬레이트를 형성하여 분자 간 상호 작용력을 증가시켜 PVC가 가소 화 효과를 발휘하고 PVC 재료의 인장 강도를 향상시키기 때문일 수 있습니다.
표 7 다양한 시료의 기계적 특성
2.5 열 안정화 메커니즘
HCl 처리 전후의 2,3⁃LPDA의 FTIR 스펙트럼은 그림 3에 나와 있습니다. 그림에서 HCl 처리 후 2,3⁃LPDA의 FTIR 스펙트럼은 처리하지 않은 것에 비해 C=N 결합의 파수가 낮은 파수에서 높은 파수로 이동했으며 처리 후 C=N 결합의 파수는 1,572 cm-1임을 알 수 있습니다. 또한 HCl 처리 후 NO3-의 텔레스코픽 진동 피크가 곡선에서 사라졌는데, 이는 H+가 NO3-와 결합하여 HNO3를 형성하기 때문입니다. 그러나 2,3⁃LPDA를 HCl로 처리 할 때 H+와 NO3-가 결합하여 HNO3를 형성하기 때문에 2,3⁃LPDA의 열 안정화 메커니즘을 결정할 수 없습니다. 2,3⁃LPDA의 HCl 처리, HCl 용액은 발열성이며 HNO3는 고온 조건에서 H2O, NO2 및 O2로 쉽게 분해되어 2,3⁃LPDA의 열 안정성 특성에 영향을 미치지 않습니다. 처리되지 않은 2,3⁃LPDA의 FTIR 스펙트럼에서 O-La 결합의 연신 진동 피크는 652 cm-1에 있습니다. 처리 후 FTIR 스펙트럼에서 O-H 결합의 두 가지 특징적인 피크, 즉 1,445 cm-1에서 O-H 결합의 신축 진동 피크와 1,097 cm-1에서 O-H 결합의 평면 외 신축 진동 피크가 더 나타났고, -COOH 결합의 특징적인 피크로 스펙트럼이 다시 나타났습니다. 이를 통해 처리 후 O-La 결합이 끊어지고 O-H 결합이 재결합되었으며, O-La 결합이 끊어진 후 La 이온이 Cl 이온과 결합하여 La-Cl 결합을 형성한 것으로 추론할 수 있으며, 처리된 2,3 ⁃LPDA의 FTIR 스펙트럼에서 1,261 cm-1의 추가 피크가 2,3 ⁃LPDA의 FTIR 스펙트럼에서 발견되었다. 처리 후 2,3⁃LPDA의 FTIR 스펙트럼에서 1,261 cm-1의 피크가 있는데, 이는 La ⁃Cl 결합의 연신 진동 피크입니다. 2,3⁃LPDA가 HCl과 반응하여 LaCl3를 형성하는 것을 알 수 있으므로 2,3⁃LPDA의 안정화 메커니즘은 2,3⁃LPDA가 PVC의 열분해 중에 방출되는 HCl 가스를 효과적으로 흡수하여 LaCl3를 형성하여 PVC의 열분해 촉매 효과를 어느 정도 지연시킬 수 있다는 것을 알 수 있습니다.
A practical selection route for photoinitiator-related projects
When technical buyers or formulators screen photoinitiators, the most useful decision frame is usually cure quality plus application fit: which package cures reliably, keeps appearance acceptable, and still works under the lamp, film thickness, and substrate conditions of the actual process.
- Match the package to the lamp first: mercury lamps, UV LEDs, and visible-light systems can rank the same photoinitiators very differently.
- Check depth cure and surface cure separately: a film that feels dry on top can still be weak underneath.
- Balance yellowing with reactivity: the strongest deep-cure route is not always the best commercial choice if color or migration risk becomes unacceptable.
- Use the final formula as the benchmark: pigment load, monomer package, and film thickness can all change the apparent ranking of the same initiator.
Recommended product references
- CHLUMINIT TPO-L: A strong low-yellowing reference for LED-oriented UV systems.
- CHLUMINIT 819: Useful when a formulation needs stronger absorption and deeper cure support.
- CHLUMINIT 184: A classic free-radical benchmark for fast surface cure in many UV systems.
- CHLUMINIT 261: A direct cationic-photoinitiator reference when cationic curing routes are being screened.
FAQ for buyers and formulators
Why are blended photoinitiator packages so common?
Because one product may control yellowing or lamp fit well while another improves cure depth or line-speed performance, so the full package is often stronger than any single grade.
Should incomplete cure always be solved by adding more initiator?
Not automatically. The real limitation may be the lamp, film thickness, pigment shading, or the rest of the reactive system rather than simple under-dosage.