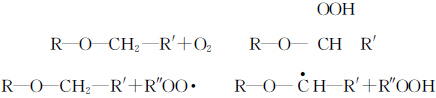Quel est l'effet du monomère UV sur le blocage de l'oxygène durcissant aux UV ?
Quick answer: For UV monomer and resin selection, the key commercial question is not “which material is best in general” but “which package delivers the right balance of flow, cure, adhesion, and durability in the real application.”
1.2 Préparation des échantillons et tests
Le monomère et l'initiateur ont été pesés avec précision, lorsque le monomère n'était pas purifié, et mélangés uniformément à l'aide d'un agitateur magnétique. L'UV-DSC a été utilisé pour réaliser des expériences de durcissement sous atmosphère statique d'air et d'azote, et les échantillons ont été prélevés en quantités égales à chaque fois, de sorte que l'épaisseur des échantillons dans le creuset était la même. Le programme UV-DSC a été réglé pour maintenir la température de l'échantillon constante pendant 2 minutes, puis la source lumineuse a été automatiquement allumée par le programme, et la lumière UV (plage de longueur d'onde 325-400 nm) a été introduite dans la cellule DSC par la fibre de verre pour éclairer le creuset de l'échantillon et le creuset de référence, et le DSC a mesuré la valeur du flux de chaleur du processus de photopolymérisation de l'échantillon. L'intensité lumineuse a été mesurée à 48,27 mW-cm-2. L'intensité lumineuse a été déterminée en étalant du noir de carbone sur le fond du creuset de l'échantillon, et l'énergie absorbée par la lumière a été mesurée par UV-DSC et divisée par la surface du fond du creuset pour obtenir l'intensité lumineuse.
2 Résultats et discussion
2.1 Traitement des données
Le taux de photopolymérisation a été calculé comme suit
Le taux de photopolymérisation R=dC/dt=(dH/dt)/Hmax, où dH/dt est la valeur du flux de chaleur sur la courbe de l'enthalpie en fonction du temps du processus de photopolymérisation mesuré par UV-DSC ; Hmax est la chaleur totale de polymérisation de l'échantillon à 200 s d'exposition à la lumière, obtenue en intégrant le pic exothermique de photopolymérisation. Le temps correspondant au taux de polymérisation maximal du processus de photopolymérisation est tmax. La polymérisation des radicaux libres se produit automatiquement de manière accélérée, la courbe du taux de photopolymérisation est dérivée du temps, la valeur maximale de la courbe correspondant au temps enregistré comme tamax, ce temps peut être considéré comme le temps de croissance le plus rapide du taux de photopolymérisation, à ce moment le système de blocage de l'oxygène et l'effet de cage et d'autres facteurs sur la consommation de radicaux primaires à un minimum. Le monomère initiateur de radicaux libres commence à polymériser rapidement.
Calcul de la teneur en initiateur (fraction molaire) α dans l'échantillon :
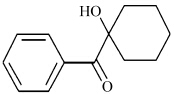
Où n initiateur est la quantité molaire d'initiateur dans le système, f est le degré fonctionnel du monomère, et n monomère est la quantité molaire de monomère dans le système. La figure 1 montre la structure moléculaire de l'initiateur Irgacure-184, qui est un type de clivage, et le "2" dans la formule (1) signifie qu'une molécule de l'initiateur peut théoriquement être décomposée en deux molécules de radicaux par exposition à la lumière.
La formule structurelle de l'Irgacure-184
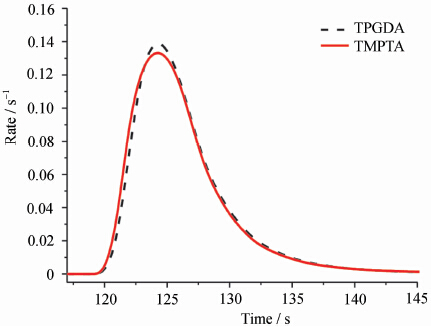
La figure 2 montre les courbes de vitesse de la photopolymérisation de différents monomères à une teneur en initiateur 4% (fraction de masse). Comme on peut le voir sur la figure, pour différents monomères, il existe des différences dans la vitesse de durcissement dans la période de prépolymérisation, et cette différence est également exprimée en temps, ce qui indique que différents monomères durcissent aux UV dans des différences de vitesse dans le temps. Le temps tamax où le taux de photopolymérisation du monomère croît le plus rapidement et le temps tmax correspondant au taux de photopolymérisation maximal sont comparés à la courbe de variation de la teneur en initiateur, et les résultats sont présentés à la figure 3.
Courbes de vitesse de durcissement aux UV de différents monomères avec l'initiateur 4%
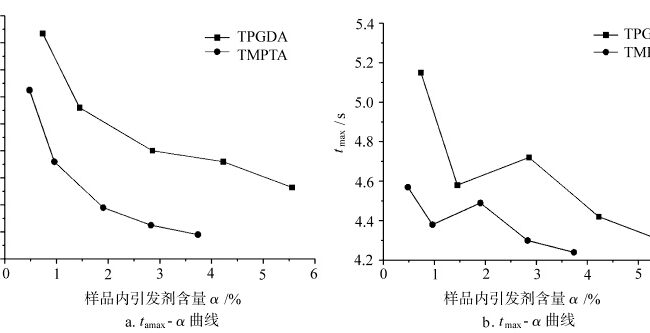
La relation entre tamax et tmax avec les teneurs en initiateurs dans le processus de durcissement à l'air de différents monomères
La figure 3 montre les courbes de tmax et tamax pour la photopolymérisation de différents monomères sous air en fonction de la teneur en initiateur α dans l'échantillon. Au début de la polymérisation, en présence d'oxygène, une partie des radicaux réactifs générés par le photo-initiateur sous l'effet de la lumière est consommée par l'oxygène dissous dans l'échantillon, et l'autre partie initie la polymérisation du monomère. L'effet de blocage de l'oxygène consomme les radicaux générés par la décomposition de l'initiateur et les radicaux monomères, affectant ainsi l'ampleur de tamax et de tmax de la photopolymérisation, ce qui reflète à son tour la sensibilité de la photopolymérisation à l'oxygène et à la teneur en initiateur. Comme le montre la figure 3a, le tamax de la photopolymérisation de chaque monomère diminue avec l'augmentation de la teneur en initiateur selon un certain schéma. Dans la figure 3b, le tmax de chaque monomère photopolymérisable montre une certaine fluctuation avec l'augmentation de la teneur en initiateur. Cela s'explique par le fait que lorsque le taux de réaction de durcissement atteint son maximum, le système a atteint un degré de durcissement élevé et les segments de la chaîne moléculaire sont progressivement gelés en raison de l'effet vitreux, et la sensibilité du tmax de la réaction de durcissement à la lumière à la teneur en initiateur est réduite à ce moment-là. Alors que le tamax, au début de la photopolymérisation, lorsque le système n'a pas un degré de polymérisation élevé, la réaction de photopolymérisation est plus sensible à la teneur de l'initiateur dans le système. Par conséquent, en comparaison, le tamax reflète mieux la sensibilité de la photopolymérisation à la teneur en initiateur.
2.2 Effet de l'atmosphère sur le tamax photopolymérisable de différents monomères
Dans une atmosphère d'air, le tamax du matériau photopolymérisé devrait être différent de celui dans une atmosphère d'azote en raison de l'effet de blocage de l'oxygène. Des tests UV-DSC ont été effectués sur le monomère TMPTA sous atmosphère d'air et d'azote lorsqu'une teneur plus faible en initiateur a été ajoutée, et les résultats sont répertoriés dans le tableau 1.
| tamaxtamax de TMPTA Durcissement aux UV avec une faible teneur en initiateurs dans l'air ou N2 | ||
| Teneur en initiateur de l'échantillon/% | tamax/s | |
| l'air | N2 | |
| 0.48 | 2.65 | 2.18 |
| 0.96 | 2.12 | 1.92 |
tamax de TMPTA durcissant aux UV avec une faible teneur en initiateurs dans l'air ou dans l'azote2
Le tableau 1 montre la comparaison du tamax du TMPTA photopolymérisé à l'air et à l'azote respectivement avec l'ajout de niveaux inférieurs d'initiateur. Le tableau ci-dessus montre que le tamax de la photopolymérisation à l'air est plus important que celui de la photopolymérisation à l'azote lorsque la teneur en initiateur est égale, ce qui indique que la photopolymérisation à l'air est affectée par le blocage de l'oxygène. On pense généralement que l'oxygène dissous dans la matière première et à la surface subit les réactions suivantes au cours du processus de photopolymérisation.
Les radicaux peroxydes ROO- générés sont très stables et n'ont pas la capacité d'initier des réactions de polymérisation. L'oxygène ne se contente pas d'éliminer les radicaux générés par l'initiateur au cours du processus de photopolymérisation, mais il met également fin aux radicaux des monomères.
La sensibilité de la photopolymérisation à la polymérisation bloquant l'oxygène varie selon les monomères et est liée à des facteurs tels que les fonctionnalités du monomère, l'activité de la double liaison et la structure [13]. Afin d'étudier l'effet de la structure du monomère sur l'agrégation bloquant l'oxygène, deux TMPTA EO-isés différents ont été sélectionnés pour des expériences UV-DSC dans des conditions d'air et d'azote, respectivement. Ces monomères homologues ont tous des structures similaires, à l'exception du nombre de groupes EO, ce qui évite de compliquer le problème en choisissant d'autres monomères avec des structures très différentes [13].
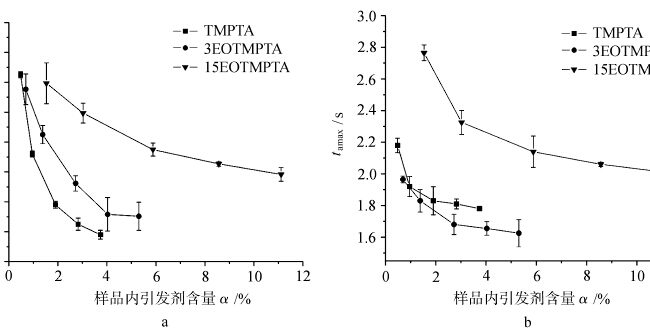
La figure 4 montre la variation du tamax en fonction de la teneur en initiateur dans l'échantillon pour la photopolymérisation de monomères TMPTA avec différentes OE sous air et azote. Comme le montre la figure, le tamax de chaque monomère photopolymérisé à l'air et à l'azote diminue avec l'augmentation de la teneur en initiateur. La variation du tamax photopolymérisé de chaque monomère sous air et azote varie avec la quantité d'OE dans le monomère. Cela montre que la quantité d'OE dans le monomère a un effet sur le tamax de la photopolymérisation. Pour un même monomère, la différence de tamax photopolymérisé sous air et sous azote est liée à la barrière d'oxygène lorsque les autres conditions sont identiques.
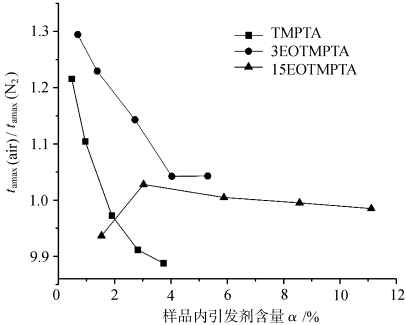
La figure 5 montre les courbes du rapport de tamax de chaque monomère photopolymérisé sous différentes atmosphères avec la variation de la teneur en initiateur α. tamax(air)/tamax(N2) indique la différence de tamax du monomère photopolymérisé sous air et sous azote, reflétant ainsi l'ampleur du blocage de l'oxygène de chaque monomère photopolymérisé, plus la valeur est grande, plus l'effet de blocage de l'oxygène est important. Comme le montre la figure 5, les rapports tamax(air)/tamax(N2) du monomère TMPTA et du monomère 3EOTMPTA étaient plus importants lorsque la teneur en initiateur était faible et diminuaient avec l'augmentation de la teneur en initiateur. Cela indique que le monomère TMPTA et le monomère 3EOTMPTA sont soumis à un effet de blocage de l'oxygène plus important lorsque la teneur en initiateur est faible. Lorsque la quantité d'OE dans le monomère atteint 15, le rapport tamax(air)/tamax(N2) du monomère est proche de 1, c'est-à-dire qu'il y a peu de différence entre le tamax(air)/tamax(N2) et le tamax(air)/tamax(N2), Il y a peu de différence dans le tamax du durcissement à la lumière dans des conditions d'air ou d'azote, ce qui indique que l'augmentation de la quantité d'OE dans le monomère est bénéfique pour réduire la polymérisation bloquant l'oxygène du durcissement aux UV, ce qui peut être lié à l'hydrogène actif dans la structure de l'OE.La structure de type éther dans la fraction OE L'α-H sur le -O-CH2- est facilement substitué par l'oxygène et les réactions suivantes se produisent.
La relation entre tamax(air)/tamax(N2) en fonction de la teneur en initateurs dans le processus de durcissement de différents TMPTA éthoxylés.
D'une part, l'α-H peut consommer une partie de l'oxygène dans le système, d'autre part, il peut mettre fin au radical peroxyde ROO- généré par le radical et l'oxygène, réduisant ainsi la consommation de radicaux réactifs et redirigeant l'activité d'initiation vers le segment de chaîne ayant une activité d'initiation, réduisant ainsi le blocage par l'oxygène du processus de photopolymérisation.
2.3 Influence de la quantité d'α-H dans les monomères sur l'agrégation de blocage de l'oxygène par photopolymérisation
Pour étudier la relation entre le blocage de l'oxygène et la quantité d'α-H dans les groupes EO monomères, les courbes tamax-α de la figure 4 ont été ajustées linéairement à différentes équations, et il a été constaté que le coefficient de corrélation le plus élevé a été obtenu en ajustant linéairement l'équation lnt=a+b/α0,5. Les pentes b obtenues à partir des ajustements et les coefficients de corrélation R sont répertoriés dans le tableau 2.
| La valeur de b et R par ajustement linéaire 1/α0,5 et lnt | ||||
| Monomère | l'air | N2 | ||
| b | R | b | R | |
| TMPTA | 0.056 | 0.99894 | 0.0213 | 0.95494 |
| EO3TMPTA | 0.0554 | 0.95877 | 0.0257 | 0.98564 |
| 15EOTMPTA | 0.0531 | 0.96578 | 0.062 | 0.98944 |
En comparant les valeurs μ correspondant à différents monomères dans la Figure 6, μ a une valeur maximale lorsque le monomère est le TMPTA, c'est-à-dire que l'effet de blocage de l'oxygène est le plus important lorsque le monomère TMPTA est polymérisé aux UV. Lorsque la quantité d'EO dans le monomère augmente, la quantité d'α-H dans le monomère augmente et la valeur μ diminue, ce qui indique que la barrière à l'oxygène est liée à la quantité d'α-H dans le monomère, qui piège l'oxygène et les radicaux peroxydes dans le système et atténue la barrière à l'oxygène. La viscosité est une propriété liée à la structure moléculaire, qui implique les propriétés d'écoulement du monomère, il est donc nécessaire de discuter davantage de l'effet des propriétés d'écoulement du monomère sur la polymérisation de la barrière à l'oxygène.
2.4 Influence des propriétés d'écoulement des monomères sur l'agrégation de la barrière à l'oxygène
Les propriétés d'écoulement du système sont liées à la structure de la molécule. En général, plus la chaîne moléculaire est souple, plus la barrière de rotation au sein de la chaîne est faible, plus le segment de chaîne est court en tant qu'unité mobile, et plus l'énergie d'activation de la chaîne moléculaire souple est faible, meilleure est la mobilité. Plus le poids moléculaire est élevé, plus la résistance interne au mouvement moléculaire due à la friction est importante et plus la mobilité est faible [19]. Par conséquent, l'introduction de groupes EO dans le monomère TMPTA modifiera les propriétés d'écoulement du système. En utilisant un rhéomètre avec un taux de cisaillement constant de 19,1 /min et un taux d'augmentation de la température de 2 °C/min, les courbes de viscosité de chaque monomère ont été mesurées en fonction de la température. Les courbes de viscosité-température de chaque monomère ont été ajustées à l'équation d'Arrhenius, et l'énergie d'activation de l'écoulement calculée E, le préfacteur A et la viscosité du monomère η à 25 ℃ ont été répertoriés dans le tableau 3.
| La valeur de la viscosité η(25 ℃), l'énergie d'activation de l'écoulement E et le facteur pré-exponentiel A des monomères. | |||
| Monomère | η/Pa-s(25℃) | A/10-8 | E/J |
| TMPTA | 0.01934 | 15.53 | 29079.88 |
| 3EOTMPTA | 0.06948 | 2.65 | 36600.47 |
| 15EOTMPTA | 0.18016 | 6.28 | 36821.87 |
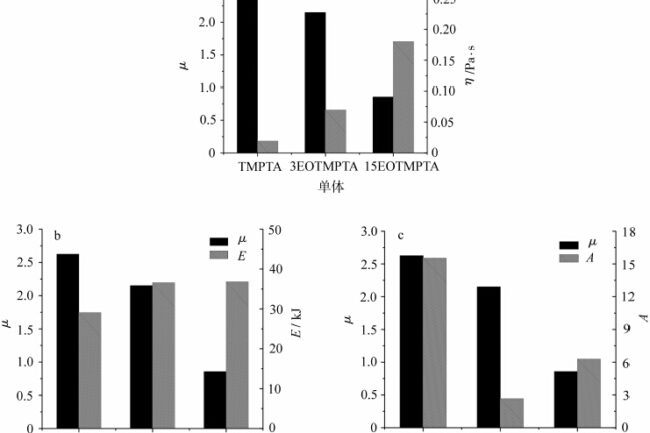
Parmi eux, l'énergie d'activation du flux E est liée à la structure moléculaire et est influencée par la rigidité et la flexibilité de la chaîne moléculaire, la taille et la polarité des groupes latéraux, etc. Le facteur de front d'indice A est une constante liée au poids moléculaire. Afin d'étudier la relation entre les propriétés d'écoulement des monomères et la barrière à l'oxygène, les valeurs μ de différents monomères ont été corrélées avec les viscosités η correspondantes, l'énergie d'activation de l'écoulement E et le préfacteur A, comme le montre la figure 7.
La figure 7 représente la comparaison des valeurs μ de différents monomères en fonction de l'énergie d'activation de l'écoulement E, du facteur de front de doigt A et de la viscosité η, respectivement. Comme le montre la figure 7a, la valeur μ tend à diminuer lorsque le nombre d'OE dans le monomère augmente et que la viscosité du monomère augmente. La taille de l'agrégation bloquant l'oxygène est étroitement liée à la concentration d'oxygène, et plus la concentration d'oxygène est importante, plus le blocage de l'oxygène est évident [7]. À l'intérieur du système de photopolymérisation, la quantité d'oxygène dissous est certaine, et le taux d'extinction et de piégeage des radicaux libres par l'oxygène dans le processus de photopolymérisation est extrêmement rapide, et l'oxygène consommé est principalement reconstitué par la diffusion de l'oxygène de l'air vers l'intérieur du système en continu, ce qui impliquera certainement la capacité de mouvement de l'oxygène dans le système, et la capacité de mouvement de l'oxygène dans le système est liée à la viscosité du système. Lorsque la viscosité du système est faible, l'oxygène de l'air est plus facile à diffuser à l'intérieur du système, montrant un effet de blocage de l'oxygène plus important, de sorte que la valeur μ du monomère TMPTA est plus élevée et est significativement bloquée par l'oxygène. Lorsque la viscosité du système augmente, la capacité de mouvement de l'oxygène dans le système diminue et il est trop tard pour reconstituer l'oxygène consommé en piégeant les radicaux libres, et le blocage de l'oxygène diminue. Comme on peut le voir sur la figure, lorsque la quantité d'OE dans le monomère augmente jusqu'à 15, la viscosité du monomère continue d'augmenter et la valeur μ tend vers 1, c'est-à-dire que la différence entre la photopolymérisation sous air et sous azote n'est pas significative.
Ensuite, comparez l'énergie d'activation de l'écoulement et le facteur de front de doigt du monomère avec la valeur μ. Comme le montre la figure 7b, l'énergie d'activation de l'écoulement du monomère augmente de TMPTA à 3EOTMPTA avec l'introduction de groupes EO dans le monomère. Lorsque la quantité d'OE dans le monomère est passée de 3 à 15, l'énergie d'activation de l'écoulement est restée pratiquement inchangée, ce qui indique que l'augmentation de la quantité d'OE dans le monomère n'a pratiquement aucun effet sur l'énergie d'activation de l'écoulement. En effet, bien que le nombre d'OE dans le monomère augmente, le nombre d'unités cinématiques ne change pas, ce qui montre que pour le monomère TMPTA OE, l'effet de l'énergie d'activation de l'écoulement sur la barrière à l'oxygène n'est pas significatif. Comme le montre la figure 7c, le préfacteur de doigt A change considérablement entre le TMPTA et le 3EOTMPTA, ce qui peut être lié à la présence ou à l'absence de groupes EO. Avec l'augmentation du nombre d'OE dans le monomère, le préfacteur A augmente, ce qui est dû à l'augmentation du nombre d'OE dans le monomère conduisant à l'augmentation du poids moléculaire du monomère. Il peut être démontré que pour les monomères TMPTA OE, l'augmentation du nombre d'OE dans la molécule entraîne une augmentation du poids moléculaire, ce qui conduit à une augmentation de la viscosité du monomère et réduit donc la barrière à l'oxygène. Pour les matériaux polymères, la viscosité du système peut généralement être augmentée en augmentant la rigidité de la chaîne moléculaire, en augmentant la polarité des groupes latéraux, en augmentant le poids moléculaire, etc. On peut supposer que les effets négatifs du blocage de l'oxygène par photopolymérisation peuvent être réduits par une composition appropriée de la formulation, telle que l'introduction de structures contenant de l'hydrogène actif, l'augmentation de la proportion de molécules rigides et l'augmentation du poids moléculaire.
3 Conclusion
(1) L'augmentation du nombre de groupes EO dans la molécule de monomère peut réduire l'agrégation bloquant l'oxygène pendant le processus de photopolymérisation. Ceci est lié au piégeage de l'oxygène et des radicaux peroxydes par les α-H de ce groupe et à l'augmentation de la viscosité du système.
(2) Pour plusieurs TMPTA OE sélectionnés pour cette étude, l'énergie d'activation de l'écoulement du monomère a peu d'effet sur l'agrégation de la barrière à l'oxygène. L'augmentation de la quantité d'OE dans le monomère entraîne une augmentation de son poids moléculaire, ce qui entraîne une augmentation de la viscosité du monomère, qui à son tour a un effet sur l'agrégation de la barrière à l'oxygène.
Monomère UV Produits de la même série
| Polythiol/Polymèrecaptan | ||
| Monomère DMES | Sulfure de bis(2-mercaptoéthyle) | 3570-55-6 |
| Monomère DMPT | THIOCURE DMPT | 131538-00-6 |
| Monomère PETMP | 7575-23-7 | |
| PM839 Monomère | Polyoxy(méthyl-1,2-éthanediyl) | 72244-98-5 |
| Monomère monofonctionnel | ||
| Monomère HEMA | Méthacrylate de 2-hydroxyéthyle | 868-77-9 |
| Monomère HPMA | Méthacrylate de 2-hydroxypropyle | 27813-02-1 |
| Monomère THFA | Acrylate de tétrahydrofurfuryle | 2399-48-6 |
| HDCPA Monomère | Acrylate de dicyclopentényle hydrogéné | 79637-74-4 |
| Monomère DCPMA | Méthacrylate de dihydrodicyclopentadiényle | 30798-39-1 |
| Monomère DCPA | Acrylate de dihydrodicyclopentadiényle | 12542-30-2 |
| Monomère DCPEMA | Méthacrylate de dicyclopentenyloxyéthyle | 68586-19-6 |
| Monomère DCPEOA | Acrylate de dicyclopentenyloxyéthyle | 65983-31-5 |
| Monomère NP-4EA | (4) nonylphénol éthoxylé | 50974-47-5 |
| Monomère LA | Acrylate de laurier / Acrylate de dodécyle | 2156-97-0 |
| Monomère THFMA | Méthacrylate de tétrahydrofurfuryle | 2455-24-5 |
| Monomère PHEA | ACRYLATE DE 2-PHÉNOXYÉTHYLE | 48145-04-6 |
| Monomère LMA | Méthacrylate de lauryle | 142-90-5 |
| Monomère IDA | Acrylate d'isodécyle | 1330-61-6 |
| Monomère IBOMA | Méthacrylate d'isobornyle | 7534-94-3 |
| Monomère IBOA | Acrylate d'isobornyle | 5888-33-5 |
| EOEOEA Monomère | Acrylate de 2-(2-Éthoxyéthoxy)éthyle | 7328-17-8 |
| Monomère multifonctionnel | ||
| Monomère DPHA | 29570-58-9 | |
| Monomère DI-TMPTA | TÉTRAACRYLATE DE DI(TRIMÉTHYLOLPROPANE) | 94108-97-1 |
| Acrylamide monomère | ||
| Monomère ACMO | 4-acryloylmorpholine | 5117-12-4 |
| Monomère di-fonctionnel | ||
| Monomère PEGDMA | Diméthacrylate de poly(éthylène glycol) | 25852-47-5 |
| Monomère TPGDA | Diacrylate de tripropylène glycol | 42978-66-5 |
| Monomère TEGDMA | Diméthacrylate de triéthylène glycol | 109-16-0 |
| Monomère PO2-NPGDA | Propoxylate de diacrylate de néopentylène glycol | 84170-74-1 |
| Monomère PEGDA | Diacrylate de polyéthylène glycol | 26570-48-9 |
| Monomère PDDA | Phtalate diacrylate de diéthylène glycol | |
| Monomère NPGDA | Diacrylate de néopentyle et de glycol | 2223-82-7 |
| Monomère HDDA | Diacrylate d'hexaméthylène | 13048-33-4 |
| Monomère EO4-BPADA | DIACRYLATE DE BISPHÉNOL A ÉTHOXYLÉ (4) | 64401-02-1 |
| EO10-BPADA Monomère | DIACRYLATE DE BISPHÉNOL A ÉTHOXYLÉ (10) | 64401-02-1 |
| EGDMA Monomère | Diméthacrylate d'éthylène glycol | 97-90-5 |
| Monomère DPGDA | Diénoate de dipropylène glycol | 57472-68-1 |
| Monomère Bis-GMA | Méthacrylate de glycidyle de bisphénol A | 1565-94-2 |
| Monomère trifonctionnel | ||
| Monomère TMPTMA | Triméthacrylate de triméthylolpropane | 3290-92-4 |
| Monomère TMPTA | Triacrylate de triméthylolpropane | 15625-89-5 |
| Monomère PETA | 3524-68-3 | |
| GPTA ( G3POTA ) Monomère | TRIACRYLATE DE GLYCÉRYLE ET DE PROPOXY | 52408-84-1 |
| Monomère EO3-TMPTA | Triacrylate de triméthylolpropane éthoxylé | 28961-43-5 |
| Monomère photorésistant | ||
| Monomère IPAMA | Méthacrylate de 2-isopropyl-2-adamantyle | 297156-50-4 |
| ECPMA Monomère | Méthacrylate de 1 éthylcyclopentyle | 266308-58-1 |
| Monomère ADAMA | Méthacrylate de 1-Adamantyle | 16887-36-8 |
| Monomère de méthacrylates | ||
| Monomère TBAEMA | Méthacrylate de 2-(Tert-butylamino)éthyle | 3775-90-4 |
| Monomère NBMA | Méthacrylate de n-butyle | 97-88-1 |
| Monomère MEMA | Méthacrylate de 2-méthoxyéthyle | 6976-93-8 |
| Monomère i-BMA | Méthacrylate d'isobutyle | 97-86-9 |
| Monomère EHMA | Méthacrylate de 2-éthylhexyle | 688-84-6 |
| Monomère EGDMP | Bis(3-mercaptopropionate) d'éthylène glycol | 22504-50-3 |
| Monomère EEMA | 2-méthoxyéthyle 2-méthylprop-2-énoate | 2370-63-0 |
| Monomère DMAEMA | Méthacrylate de N,M-diméthylaminoéthyle | 2867-47-2 |
| Monomère DEAM | Méthacrylate de diéthylaminoéthyle | 105-16-8 |
| Monomère CHMA | Méthacrylate de cyclohexyle | 101-43-9 |
| Monomère BZMA | Méthacrylate de benzyle | 2495-37-6 |
| Monomère BDDMP | 1,4-Butanediol Di(3-mercaptopropionate) | 92140-97-1 |
| Monomère BDDMA | 1,4-Butanedioldiméthacrylate | 2082-81-7 |
| Monomère AMA | Méthacrylate d'allyle | 96-05-9 |
| Monomère AAEM | Méthacrylate d'acétylacétoxyéthyle | 21282-97-3 |
| Monomère d'acrylates | ||
| Monomère IBA | Acrylate d'isobutyle | 106-63-8 |
| Monomère EMA | Méthacrylate d'éthyle | 97-63-2 |
| Monomère DMAEA | Acrylate de diméthylaminoéthyle | 2439-35-2 |
| Monomère DEAEA | 2-(diéthylamino)éthyl prop-2-énoate | 2426-54-2 |
| Monomère CHA | Prop-2-énoate de cyclohexyle | 3066-71-5 |
| Monomère BZA | prop-2-énoate de benzyle | 2495-35-4 |
How buyers usually evaluate UV monomers and resin systems
Most successful UV formulations are built by choosing the backbone first and then tuning the reactive monomer package around the substrate, cure method, and end-use stress. That usually produces a more stable result than choosing materials by viscosity or price alone.
- Start from the final property target: hardness, flexibility, adhesion, and shrinkage rarely point to exactly the same raw-material package.
- Screen the reactive package as a whole: oligomer, monomer, and photoinitiator choices interact strongly in UV systems.
- Use viscosity as a tool, not the only decision rule: the easiest-processing material is not always the one that performs best after cure.
- Check the real substrate: plastic, metal, label film, gel systems, and coatings can reward very different polarity and cure-density balances.
Recommended product references
- CHLUMINIT 184: A classic free-radical benchmark for fast surface cure in many UV systems.
- CHLUMINIT TMO: A valuable comparison point when lower yellowing or TPO-replacement discussions matter.
- CHLUMICRYL HPMA: Useful when more polarity and adhesion support are needed in the reactive package.
- CHLUMICRYL IBOA: A strong low-viscosity monomer reference when hardness and good flow both matter.
FAQ for buyers and formulators
Can one UV monomer or resin solve every formulation problem?
Usually no. Commercially strong formulas depend on how several components work together to balance cure, adhesion, flow, and durability.
Why should monomers be screened together with oligomers?
Because monomers can change viscosity, cure rate, shrinkage, and substrate behavior enough to alter the final ranking of the same backbone resin.