PVC adalah salah satu polimer yang paling banyak digunakan di pasaran saat ini, dan memainkan peran penting dalam bidang bahan konstruksi dan kemasan elektronik. Namun, PVC dalam faktor eksternal (seperti panas, oksigen, cahaya dan gaya, dll.) Di bawah aksi degradasi dan reaksi ikatan silang, mengakibatkan perubahan warna produk PVC, melemahnya sifat mekanik. PVC yang dipanaskan hingga 110℃ akan melepaskan gas HCl, sehingga PVC mulai terurai. Saat ini, penstabil panas PVC terutama terdiri dari lima jenis: penstabil panas garam timbal, penstabil panas sabun logam, penstabil panas organotin, penstabil panas organik, dan penstabil panas tanah jarang. Karena stabilisator panas garam timbal memiliki logam berat, pencemaran lingkungan yang serius, sekarang jarang digunakan. Stabilisator panas jenis sabun logam awalnya memiliki kemampuan anti-warna yang buruk, degradasi PVC dari kemampuan substitusi atom klorin yang tidak stabil buruk, untuk memenuhi permintaan pasar. Stabilisator panas timah organik memiliki efek stabilisasi yang signifikan, tetapi beberapa di antaranya beracun dan berbiaya tinggi, yang membatasi perkembangannya. Stabilisator panas organik tidak beracun dan ramah lingkungan, tetapi stabilitas stabilisator panas PVC saja buruk. Stabilisator panas tanah jarang telah dipelajari lebih banyak, yang memiliki keunggulan toksisitas rendah, perlindungan lingkungan, dan stabilitas termal yang baik.
Dengan perkembangan dan inovasi ilmu pengetahuan dan teknologi, perlindungan lingkungan telah menjadi kriteria penting untuk penstabil panas, sehingga penstabil panas asam karboksilat heterosiklik yang mengandung nitrogen telah mendapat perhatian luas. Ini karena komposisi penstabil panas tidak mengandung logam berat, yang memecahkan masalah polusi, dan juga merupakan ligan yang sangat baik dengan stabilitas termal yang baik. Dengan menggabungkan penstabil panas asam karboksilat heterosiklik yang mengandung nitrogen dengan larutan garam tanah jarang, penstabil panas asam karboksilat heterosiklik asam heterosiklik yang mengandung nitrogen dapat disintesis. Keunggulannya adalah toksisitas rendah, perlindungan lingkungan, transmisi cahaya yang baik, stabilitas termal yang baik, biaya rendah, hasil tinggi, dan potensi pengembangan yang tinggi. Liu Zhaogang et al. menggunakan imidazol ⁃ 4,5 ⁃ asam dikarboksilat, natrium hidroksida, lantanum klorida sebagai bahan baku untuk membuat penstabil panas asam karboksilat heterosiklik asam heterosiklik yang mengandung nitrogen, dan kemudian menggunakan eksperimen stabilisasi panas statis dan eksperimen stabilisasi panas dinamis untuk melakukan studi lebih lanjut, dan menemukan bahwa proses preparasi relatif tidak praktis dan waktu reaksinya relatif lama, namun produk dari stabilitas termal kompleks tersebut masih baik. Zhang Ning dan yang lainnya mensintesis 8 jenis penstabil panas asam amino lantanum dengan asam amino, natrium hidroksida dan lantanum nitrat sebagai bahan baku, dan dipelajari lebih lanjut dengan eksperimen stabilisasi panas statis dan eksperimen stabilisasi panas dinamis, serta membandingkan stabilitas panas 8 jenis asam amino lantanum, dan menemukan bahwa 8 jenis asam amino lantanum mengandung cincin benzena dan belerang, yang beracun dan tidak ramah lingkungan, dan triptofan di antara 8 jenis bahan baku asam amino mengandung cincin benzena, tetapi stabilitas panas triptofan lantanum lebih baik dari pada 8 jenis asam amino, dan stabilitas panas triptofan lantanum lebih baik dari pada 8 jenis asam amino. Namun, stabilitas termal triptofan lantanum adalah yang terbaik di antara 8 jenis asam amino lantanum, dan energi aktivasi penstabil panas senyawanya lebih baik daripada monomer lantanum triptofan dan penstabil panas kalsium dan seng yang tersedia secara komersial, yang dapat meningkatkan stabilitas termal PVC.
Dalam makalah ini, 2,3⁃PDA disintesis sebagai ligan elemen lantanum pada pH = 6 ~ 7. 2,3⁃LPDA digunakan sebagai penstabil panas utama PVC untuk studi stabilitas panas, dan kemudian digabungkan dengan penstabil panas tambahan seperti kalsium stearat, seng stearat, pentaeritritol, dll, dan stabilitas panas dari sistem majemuk dianalisis secara komparatif dengan 2,3⁃LPDA dan stabilisasi termal dari bagian panas Efek dari beberapa penstabil panas pada sifat plastisisasi dan mekanik PVC dikarakterisasi; akhirnya, mekanisme stabilisasi panas 2,3⁃LPDA diselidiki.
1
Persiapan Sampel
2,3⁃ Persiapan LPDA: timbang jumlah lantanum oksida yang sesuai ke dalam gelas kimia, tambahkan air deionisasi dan aduk rata; masukkan gelas kimia ke dalam pemanas penangas air 60℃, aduk larutan berair lantanum oksida dengan pengaduk, lalu gunakan pipet untuk perlahan-lahan menambahkan larutan asam nitrat ke larutan lantanum oksida yang benar-benar larut; nilai pH larutan ditentukan menjadi 3 ~ 4 dengan kertas pH untuk filtrasi, filtrat yang diperoleh untuk larutan lantanum nitrat, dan dituangkan ke dalam botol reagen untuk cadangan, dan nilai molarnya adalah 0.015 mg / L. Larutan tersebut disaring dan kemudian dituangkan ke dalam botol reagen. Botol reagen cadangan, konsentrasi molarnya ditentukan dengan titrasi EDTA; menimbang rasio molar 3:2 2,3 ⁃ PDA dan lantanum nitrat, etanol anhidrat pertama akan menjadi 2,3 ⁃ bubuk PDA yang dilarutkan, lalu encerkan amonia untuk menyesuaikan pH menjadi 6 ~ 7, dalam pengadukan konstan larutan lantanum nitrat secara perlahan ditambahkan ke larutan etanol anhidrat 2,3 ⁃ PDA, dan kemudian encerkan amonia untuk menyesuaikan pH sistem menjadi 6 ~ 7, menghasilkan endapan putih, dengan pengaduk listrik. Endapan putih, diaduk dengan pengaduk listrik selama 3 jam untuk membuat sistem sepenuhnya reaktif, dan kemudian dibiarkan agar endapan mengendap semua diendapkan, dan kemudian disaring, dan kemudian dicuci endapan dengan etanol anhidrat selama beberapa kali; komposit dikeringkan pada suhu 50 ℃ hingga berat konstan, dan produk yang dihasilkan adalah 2,3 ⁃ penstabil panas tanah jarang LPDA, dan kemudian produk tersebut digiling menjadi bubuk dan kemudian dimasukkan ke dalam kantong untuk penggunaan cadangan;
Persiapan penstabil panas majemuk: 2,3 ⁃ LPDA dengan seng stearat dan pentaeritritol sesuai dengan rasio massa yang berbeda dari peracikan biner dan terner, menimbang, menggiling, dan mencampur bubuk, mengantongi cadangan.
2
Hasil dan Pembahasan
2.1 Karakterisasi 2,3⁃LPDA
2.1.1 Analisis spektral inframerah
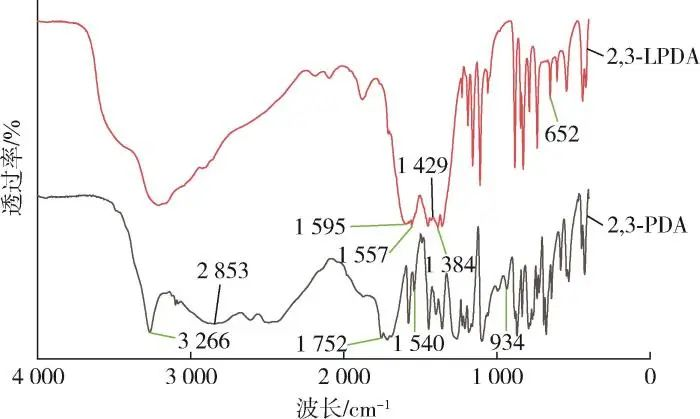
Gambar 1 menunjukkan spektrum FTIR dari 2,3⁃PDA dan 2,3⁃LPDA. Dapat dilihat bahwa puncak-puncak vibrasi teleskopik ikatan C=N pada 2,3⁃PDA dan 2,3⁃LPDA masing-masing pada 1.540 cm-1 dan 1.557 cm-1 ; puncak-puncak vibrasi teleskopik NO3- pada 2,3⁃LPDA pada 1.384 cm-1 ; puncak-puncak vibrasi teleskopik ikatan C=O pada 2,3⁃PDA pada 1.752 cm-1 ; puncak-puncak vibrasi teleskopik ikatan C=O pada 2,3⁃PDA masing-masing pada 1.595 cm-1 dan 1.429 cm-1 ; puncak-puncak vibrasi teleskopik ikatan C=O pada 2,3⁃PDA masing-masing pada 1.595 cm-1 dan 1.429 cm-1 pada 1.595 cm-1 dan 1.429 cm-1 adalah puncak getaran teleskopik antisimetris dan simetris dari ikatan C=O pada 2,3 ⁃PDA, masing-masing; 3.266 cm-1 adalah puncak getaran teleskopik ikatan O-H pada 2,3 ⁃PDA; dan 934 cm-1 adalah puncak karakteristik -COOH pada 2,3 ⁃PDA, yang memungkinkan kami untuk menentukan bahwa gugus karboksilat hadir; Puncak vibrasi regangan ikatan O-La pada 2,3⁃LPDA pada 652 cm-1 , dengan demikian menunjukkan bahwa reaksi 2,3⁃PDA dengan ligan lantanum nitrat menyebabkan ikatan O-H pada gugus karboksilat pada 2,3⁃PDA memutus rantai dan de-H, dan membentuk ikatan O-La dengan ion La. Secara ringkas, dapat ditentukan bahwa reaksi tersebut menghasilkan 2,3⁃LPDA.
Gambar 1 Spektrum FTIR sampel
2.1.2 Analisis elemen dan termal
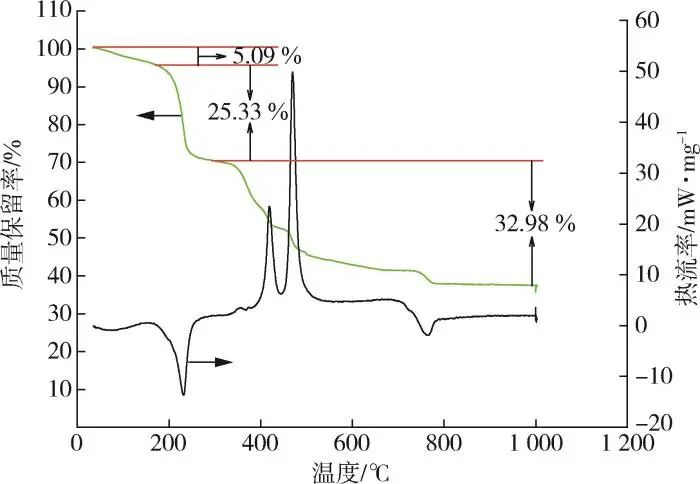
Kandungan unsur C, H dan N dalam 2,3⁃LPDA ditentukan dengan analisis unsur, dan kandungan lantanum ditentukan dengan titrasi EDTA. Melalui Tabel 1, dapat dilihat bahwa kesalahan relatif kandungan unsur H (fraksi massa, sama di bawah) besar karena jumlahnya yang kecil, dan kandungan aktual unsur lainnya pada dasarnya konsisten dengan kandungan teoritis. Kemudian jumlah air kristalisasi dihitung dengan hasil analisis termal pada Gbr. 2, yang mengarah pada rumus molekul 2,3⁃LPDA sebagai La2(C6N2O4)2(NO3)2-3H2O. Dari kurva TG pada Gbr. 2, dapat dilihat bahwa penurunan berat termal 2,3⁃LPDA dibagi menjadi tiga fase, yaitu fase dari 50 hingga 184, 184 hingga 292, dan 292 hingga 1.000 ℃, masing-masing. Laju kehilangan massa pada tahap pertama adalah 5,09 %, dan dari laju kehilangan massa tersebut, disimpulkan bahwa ada tiga air kristal, yang mirip dengan 6.88 % kandungan air kristal dalam rumus molekul La2 (C6N2O4) 2 (NO3) 2-3H2O seperti yang disimpulkan dari Tabel 1; kurva DSC tahap pertama memiliki puncak penyerapan panas pada 87,1 ~ 140,6 ℃, yang mewakili penghilangan air kristal dari 2,3 ⁃ LPDA. Dari kurva TG tahap kedua dan ketiga, dapat dilihat bahwa 2,3 ⁃LPDA menunjukkan penurunan berat badan yang tajam, dengan total kehilangan massa 58,31% pada tahap kedua dan ketiga; berbeda dengan kurva DSC, terdapat puncak inspirasional 184 ~ 292,4 ℃ pada tahap kedua, yang merepresentasikan penguraian produk. Dua puncak eksotermis muncul pada tahap ketiga, yang mewakili dekomposisi lebih lanjut dari produk. Setelah 797 ℃, tidak ada penurunan berat badan lebih lanjut, dan kurva TG cenderung mendatar, dan residu akhirnya adalah La2O3, yang menyumbang 36.59% dari fraksi massa, dan kandungan La dihitung menjadi 31.11%, yang mirip dengan kandungan La teoritis 31.53% pada Tabel 1. Singkatnya, rumus molekul penstabil panas tanah jarang ditentukan sebagai La2(C6N2O4)2(NO3)2-3H2O dengan membandingkan data pada Tabel 1 dan Gambar 2.
Tabel 1 Hasil analisis unsur 2,3⁃LPDA
Gbr. 2 Kurva analisis termal 2,3⁃LPDA
2.2 Analisis stabilitas termal
2.2.1 Penstabil termal tunggal
Untuk dapat mempelajari stabilitas termal 2,3⁃LPDA secara lebih mendalam, stabilitas termalnya dibandingkan dengan stabilisator termal yang umum, dan hasilnya ditunjukkan pada Tabel 2. Menurut Tabel 2, dapat dilihat bahwa waktu stabilisasi termal 2,3⁃LPDA adalah 30 menit, yang 6 kali lebih lama dari 2,3⁃PDA, hanya lebih pendek dari pada timbal stearat, dan lebih lama dari pada penstabil panas lainnya dalam tabel. Dalam hal kinerja anti-pewarnaan, 2,3⁃LPDA memiliki kinerja anti-pewarnaan awal yang lebih baik daripada 2,3⁃PDA, yang menunjukkan bahwa 2,3⁃LPDA memiliki kemampuan pengikatan yang lebih kuat dengan Cl- yang tidak stabil, dan meningkatkan kinerja anti-pewarnaan awal PVC. Dalam hal kinerja anti-pewarnaan jangka panjang, 2,3⁃LPDA sedikit lebih lemah daripada kalsium stearat dan pentaeritritol dalam kemampuan anti-pewarnaan. Kecuali kalsium stearat dan pentaeritritol, 2,3⁃LPDA memiliki beberapa keunggulan dibandingkan penstabil panas lainnya dalam kinerja anti-pewarnaan, dan memiliki efek positif dalam mencegah degradasi termal PVC.
Tabel 2 Stabilitas termal dari berbagai penstabil panas
2.2.2 2,3⁃LPDA yang diracik dengan seng stearat
Resistensi perubahan warna awal 2,3⁃LPDA sedikit lebih buruk daripada seng stearat, tetapi waktu stabilisasi termal dan ketahanan perubahan warna jangka panjangnya jauh lebih baik daripada seng stearat. Hasil uji stabilitas termal dari kedua kompleks ditunjukkan pada Tabel 3. Dari Tabel 3, dapat dilihat bahwa waktu stabilitas termal terlama adalah 34 menit ketika rasio peracikan 2,3⁃LPDA dan seng stearat adalah 4: 1, dan lebih lama dari itu ketika 2,3⁃LPDA digunakan sebagai penstabil termal saja, dan semakin besar proporsi 2,3⁃LPDA dalam rasio peracikan, semakin lama waktu stabilitas termal. Hal ini karena Re3+ dan Cl- memiliki efek koordinasi yang kuat dan akan lebih mudah berkoordinasi dengan Cl- yang terurai oleh panas. Dalam hal kinerja anti perubahan warna, kinerja anti perubahan warna awal dari penstabil panas majemuk sangat meningkat. Ini karena 2,3 ⁃ penghambatan awal LPDA dari seng stearat untuk menghasilkan fenomena "pembakaran seng" terlihat jelas, dan ada efek sinergis yang kuat, peracikan kinerja anti-warna awal PVC telah sangat ditingkatkan. Namun, dari kinerja anti-pengubahan warna jangka panjang, 2,3 ⁃ LPDA saja lebih baik daripada kinerja anti-pengubahan warna yang diperparah, dan 2,3 ⁃ LPDA dalam rasio peracikan dengan proporsi yang lebih kecil, fenomena "pembakaran seng" akan lebih terlihat, semakin buruk anti-pengubahan warna jangka panjang, semakin pendek waktu stabilisasi panas, menunjukkan bahwa semakin banyak proporsi seng stearat dalam rasio peracikan semakin banyak, semakin banyak proporsi 2,3 ⁃ LPDA dan seng stearat, dan semakin banyak proporsi 2,3 ⁃ LPDA dan seng stearat, semakin banyak proporsi 2,3 ⁃ LPDA dan seng stearat. Semakin pendek waktu stabilisasi panas, menunjukkan bahwa semakin besar proporsi seng stearat dalam rasio peracikan, semakin buruk efek sinergis antara LPDA dan seng stearat.
Tabel 3 Stabilitas termal dari sistem senyawa seng stearat
2.2.3 Peracikan 2,3⁃LPDA dengan Pentaeritritol
Pentaeritritol adalah penstabil panas tambahan dengan stabilitas termal yang sangat baik, dan kinerja anti perubahan warna jangka pendek dan jangka panjangnya bagus. 2,3⁃LPDA dan pentaeritritol yang dikomplekskan dengan stabilitas termal ditunjukkan pada Tabel 4. Dari tabel tersebut, dapat dilihat bahwa waktu stabilitas termal dari dua penstabil panas yang dikomplekskan berada pada kisaran 31-34 menit, dan waktu stabilitas termal 2,3 ⁃ LPDA sebagai penstabil panas saja adalah 30 menit, yang menunjukkan bahwa waktu stabilitas termal 2,3 ⁃LPDA dengan pentaeritritol yang dikomplekskan dengan seng stearat adalah 30 menit, yang menunjukkan bahwa efek sinergis antara 2,3 ⁃LPDA dan seng stearat semakin penting. 3⁃LPDA dan efek stabilisasi panas peracikan pentaeritritol tidak jelas, waktu stabilisasi panas hanya diperpanjang 1-3 menit, tetapi juga memiliki efek sinergis tertentu. Dalam hal kinerja anti perubahan warna, efek pentaeritritol sangat jelas, dan kinerja anti perubahan warna awal dari kedua komposit lebih baik daripada 2,3⁃LPDA saja sebagai penstabil panas. Dari kinerja anti-warna jangka panjang, semakin besar proporsi pentaeritritol dalam penstabil panas majemuk, semakin baik kemampuan anti-warna jangka panjang, yang menunjukkan bahwa peracikan pentaeritritol dan 2,3⁃ LPDA memiliki kinerja anti-warna yang baik, dan pentaeritritol semakin meningkatkan kinerja anti-warna jangka panjang 2,3⁃ LPDA. Secara keseluruhan, efek stabilisasi panas pentaeritritol tidak terlihat jelas, tetapi sifat anti perubahan warna sangat menonjol. Hal ini disebabkan oleh kemampuan alkohol untuk mengubah warna PVC saat dipanaskan, dan saat suhu meningkat, alkohol mengalami esterifikasi, sehingga lebih sulit bagi alkohol untuk mengendap dari PVC. Pada saat yang sama, pentaeritritol dan lantanum dapat dikomplekskan untuk menebus rantai yang rusak dalam rantai molekul selama degradasi PVC, sehingga meningkatkan kemampuan perubahan anti-warna jangka panjang PVC.
Tabel 4 Stabilitas termal sistem kompleks pentaeritritol
2.2.4 Peracikan 2,3⁃LPDA, seng stearat, dan pentaeritritol
Fenomena "seng terbakar" yang disebabkan oleh seng stearat dapat ditunda oleh pentaeritritol. Untuk membuat penstabil panas memiliki kemampuan perubahan anti-warna yang lebih baik dan waktu stabilisasi panas, 2,3⁃LPDA, seng stearat dan pentaeritritol diracik, dan stabilitas panasnya ditunjukkan pada Tabel 5. Seperti yang ditunjukkan pada Tabel 5, ketika rasio 2,3⁃LPDA: seng stearat: pentaeritritol adalah 2: 1: 2, waktu stabilisasi termal adalah 44 menit, yang lebih tinggi daripada dua set rasio peracikan lainnya, yang sepenuhnya membuktikan bahwa ada efek sinergis yang kuat ketika 2,3⁃LPDA dan pentaeritritol memiliki proporsi yang sama. Dari pandangan kinerja anti-pengubahan warna, karena penambahan pentaeritritol, anti-pengubahan warna dari sistem yang diperparah telah sangat ditingkatkan, dan pentaeritritol juga memperlambat terjadinya fenomena seng stearat "luka bakar seng", anti-pengubahan warna jangka panjang dari sistem setelah tiga peracikan telah meningkat secara signifikan. Dengan membandingkan Tabel 2, Tabel 3 dan Tabel 5, dapat dilihat bahwa kinerja anti-pewarnaan dari sistem peracikan terner jauh lebih baik daripada peracikan biner. Hal ini karena, sampai batas tertentu, penstabil panas tambahan poliol dapat mencegah terjadinya fenomena "pembakaran seng" seng stearat, dan kompleks yang dihasilkan oleh reaksi antara pentaeritritol dan seng stearat dapat secara efektif melemahkan efek katalitik ZnCl2 pada degradasi PVC.
Tabel 5 Stabilitas termal sistem peracikan terner
2.3 Analisis sifat plastisisasi
Dalam penelitian ini, percobaan plastisisasi dilakukan pada penstabil panas yang berbeda untuk mempelajari efek penstabil panas pada stabilitas termal dinamis PVC, dan hasilnya ditunjukkan pada Tabel 6. Seperti yang dapat dilihat dari tabel, waktu plastisisasi sampel penstabil panas yang mengandung seng stearat yang dicampur dengan 2,3⁃ LPDA adalah yang paling lama. Hal ini karena seng stearat saja yang plastisisasi, kinerja plastisisasi sangat buruk, pada akhir pengisian, akan segera muncul fenomena "pembakaran seng", fenomena tersebut akan mendorong degradasi PVC, tidak dapat mewujudkan plastisisasi; dan dengan kompleks 2,3 ⁃ LPDA, 2,3 ⁃ LPDA berperan dalam memperlambat fenomena "pembakaran seng", efek dari fenomena "pembakaran seng", efek dari fenomena "pembakaran seng". "Setelah puncak plastisisasi, seng stearat mulai mendorong degradasi PVC, yang menyebabkan percepatan dekomposisi bubuk PVC. Meskipun waktu plastisisasi sampel yang mengandung penstabil panas terner sedikit lebih lama dibandingkan dengan sampel yang mengandung 2,3 ⁃ LPDA, torsi plastisisasi dan torsi kesetimbangannya lebih rendah, yang mengindikasikan bahwa hal itu dapat mengurangi daya rekat antara PVC dan mesin pengolah selama proses berlangsung, sehingga mengurangi kehilangan energi dan konsumsi daya.
Tabel 6 Sifat-sifat plastisisasi dari sampel yang berbeda
2.4 Analisis sifat tarik
Menurut hasil percobaan stabilisasi panas statis, stabilisator panas tanah jarang dengan kinerja stabilisasi panas terbaik di setiap kelompok percobaan dipilih untuk uji sifat tarik untuk mempelajari pengaruh stabilisator panas yang berbeda pada sifat tarik PVC, dan hasilnya ditunjukkan pada Tabel 7. Hasilnya ditunjukkan pada Tabel 7. Dari tabel tersebut, dapat dilihat bahwa sifat tarik PVC meningkat secara signifikan setelah 2,3⁃LPDA ditambahkan ke PVC; perbedaan sifat tarik antara sampel penstabil panas yang mengandung 2,3⁃LPDA dan seng stearat dan sifat tarik sampel yang mengandung 2,3⁃LPDA sangat besar, yang mungkin disebabkan oleh fakta bahwa beberapa seng stearat tampaknya memiliki fenomena "seng terbakar" saat mencampurkan lembaran PVC, yang mendorong degradasi PVC. Hal ini mungkin disebabkan oleh fenomena "seng terbakar" dari beberapa seng stearat selama pencampuran serpihan PVC, yang mendorong degradasi PVC dan mengurangi kekuatan tarik serpihan PVC, yang mengakibatkan buruknya sifat mekanik serpihan PVC. Data terakhir pada Tabel 7 menunjukkan bahwa 2,3⁃LPDA, seng stearat dan pentaeritritol memiliki efek terbaik pada peningkatan kekuatan tarik PVC. Hal ini mungkin disebabkan karena unsur tanah jarang memiliki banyak orbital kosong untuk menerima elektron tunggal ligan, sedangkan ion logam tanah jarang memiliki jari-jari ionik yang besar, sehingga ia dan zat organik dan anorganik dalam formula PVC membentuk berbagai ligan atau kelat, meningkatkan gaya interaksi antarmolekul, PVC memainkan efek plastisisasi, dan meningkatkan kekuatan tarik bahan PVC.
Tabel 7 Sifat mekanis dari sampel yang berbeda
2.5 Mekanisme stabilisasi panas
Spektra FTIR 2,3⁃LPDA sebelum dan sesudah perlakuan HCl ditunjukkan pada Gambar 3. Dari gambar tersebut, dapat dilihat bahwa spektra FTIR 2,3⁃LPDA setelah perlakuan HCl menggeser bilangan gelombang ikatan C=N dari bilangan gelombang rendah ke bilangan gelombang tinggi dibandingkan dengan yang tidak diberi perlakuan, dan bilangan gelombang ikatan C=N setelah perlakuan adalah 1.572 cm-1 . Selain itu, puncak vibrasi teleskopik NO3- menghilang dari kurva setelah perlakuan dengan HCl karena fakta bahwa H+ bergabung dengan NO3- membentuk HNO3. Namun, karena kombinasi H+ dan NO3- membentuk HNO3 pada perlakuan 2,3⁃LPDA dengan HCl, maka mekanisme stabilisasi termal 2,3⁃LPDA tidak dapat ditentukan. Perlakuan HCl terhadap 2,3⁃LPDA, larutan HCl bersifat eksotermik, sedangkan HNO3 mudah terurai menjadi H2O, NO2, dan O2 dalam kondisi suhu tinggi, yang tidak mempengaruhi sifat stabilitas termal 2,3⁃LPDA. Dalam spektrum FTIR 2,3⁃LPDA yang tidak diberi perlakuan, puncak vibrasi regangan ikatan O-La berada pada 652 cm-1. Setelah perlakuan, terdapat dua puncak karakteristik ikatan O-H dalam spektra FTIR, yaitu puncak vibrasi teleskopik ikatan O-H pada 1.445 cm-1 dan puncak vibrasi teleskopik di luar bidang ikatan O-H pada 1.097 cm-1 , dan, spektra muncul kembali dengan puncak karakteristik ikatan - COOH. Dari penjelasan di atas, dapat disimpulkan bahwa ikatan O-La terputus dan ikatan O-H digabungkan kembali setelah perlakuan, dan setelah ikatan O-La terputus, ion La bergabung dengan ion Cl untuk membentuk ikatan La-Cl, dan dari spektrum FTIR 2,3 ⁃LPDA yang diberi perlakuan, puncak tambahan pada 1.261 cm-1 ditemukan pada spektrum FTIR 2,3 ⁃LPDA. Dari spektrum FTIR 2,3-LPDA setelah perlakuan, terdapat puncak 1.261 cm-1 yang merupakan puncak vibrasi regangan dari ikatan La ⁃Cl. Terlihat bahwa 2,3⁃LPDA bereaksi dengan HCl membentuk LaCl3, sehingga dapat diketahui bahwa mekanisme penstabilan 2,3⁃LPDA adalah 2,3⁃LPDA secara efektif dapat menyerap gas HCl yang dilepaskan selama degradasi termal PVC dan membentuk LaCl3, yang dapat menunda efek katalitik degradasi termal PVC sampai batas tertentu.