Le PVC est l'un des polymères les plus utilisés sur le marché aujourd'hui, et il joue un rôle important dans les domaines des matériaux de construction et de l'emballage électronique. Cependant, sous l'action de facteurs externes (tels que la chaleur, l'oxygène, la lumière et la force, etc.), le PVC subit une dégradation et une réaction de réticulation, ce qui entraîne une décoloration des produits en PVC et un affaiblissement de leurs propriétés mécaniques.Le PVC chauffé à 110 ℃ libère du gaz HCl, de sorte que le PVC commence à se décomposer. À l'heure actuelle, les stabilisateurs thermiques du PVC sont principalement de cinq types : les stabilisateurs thermiques à base de sels de plomb, les stabilisateurs thermiques à base de savon métallique, les stabilisateurs thermiques à base d'organoétain, les stabilisateurs thermiques organiques et les stabilisateurs thermiques à base de terres rares. Les stabilisateurs thermiques à base de sels de plomb contiennent des métaux lourds et polluent gravement l'environnement, c'est pourquoi ils sont désormais rarement utilisés. Les stabilisants thermiques de type savon métallique ont initialement une faible capacité anti-coloration, la capacité de substitution de l'atome de chlore instable par le PVC est faible, pour répondre à la demande du marché. Les stabilisants thermiques organiques à base d'étain ont un effet stabilisant important, mais certains d'entre eux sont toxiques et coûteux, ce qui limite leur développement. Les stabilisateurs thermiques organiques sont non toxiques et respectueux de l'environnement, mais la stabilité des stabilisateurs thermiques en PVC seul est médiocre. Les stabilisateurs thermiques à base de terres rares ont fait l'objet d'études plus approfondies et présentent les avantages d'une faible toxicité, d'une protection de l'environnement et d'une bonne stabilité thermique.
Avec le développement et l'innovation de la science et de la technologie, la protection de l'environnement est devenue un critère important pour les stabilisateurs thermiques, de sorte que les stabilisateurs thermiques à base d'acide carboxylique hétérocyclique contenant de l'azote ont reçu une grande attention. En effet, la composition du stabilisateur thermique ne contient pas de métaux lourds, ce qui résout le problème de la pollution, et c'est également un excellent ligand doté d'une bonne stabilité thermique. En combinant les stabilisateurs thermiques à base d'acide carboxylique hétérocyclique contenant de l'azote avec une solution de sel de terre rare, il est possible de synthétiser un nouveau type de stabilisateur thermique à base d'acide carboxylique hétérocyclique contenant de l'azote et de terre rare. Ses avantages sont les suivants : faible toxicité, protection de l'environnement, bonne transmission de la lumière, bonne stabilité thermique, faible coût, rendement élevé et fort potentiel de développement. Liu Zhaogang et al. ont utilisé l'acide imidazole ⁃ 4,5 ⁃ dicarboxylique, l'hydroxyde de sodium et le chlorure de lanthane comme matières premières pour préparer un stabilisateur thermique à base d'acide carboxylique hétérocyclique contenant de l'azote et des terres rares, puis ont utilisé des expériences de stabilisation thermique statique et des expériences de stabilisation thermique dynamique pour mener une étude plus approfondie, et ont constaté que le processus de préparation est relativement lourd et que le temps de réaction est relativement long, mais que le produit de la stabilité thermique du complexe est toujours bon. Zhang Ning et d'autres ont synthétisé 8 types de stabilisants thermiques à base d'acides aminés, d'hydroxyde de sodium et de nitrate de lanthane comme matières premières, et ont réalisé des expériences de stabilisation thermique statique et des expériences de stabilisation thermique dynamique, et ont comparé la stabilité thermique de 8 types d'acides aminés à base de lanthane, Il a été constaté que les 8 types d'acides aminés de lanthane contenaient un anneau de benzène et du soufre, qui étaient toxiques et non respectueux de l'environnement, et que le tryptophane parmi les 8 types de matières premières d'acides aminés contenait un anneau de benzène, mais que la stabilité thermique du tryptophane de lanthane était meilleure que celle des 8 types d'acides aminés, et que la stabilité thermique du tryptophane de lanthane était meilleure que celle des 8 types d'acides aminés. Toutefois, la stabilité thermique du tryptophane de lanthane est la meilleure parmi les 8 types d'acides aminés de lanthane, et l'énergie d'activation de son stabilisateur thermique composé est meilleure que celle du monomère de tryptophane de lanthane et des stabilisateurs thermiques de calcium et de zinc disponibles dans le commerce, ce qui peut améliorer la stabilité thermique du PVC.
Dans cet article, le 2,3⁃PDA a été synthétisé comme ligand de l'élément lanthane à pH=6~7. Le 2,3⁃LPDA a été utilisé comme stabilisateur thermique principal du PVC pour l'étude de la stabilité thermique, puis il a été composé avec des stabilisateurs thermiques auxiliaires tels que le stéarate de calcium, le stéarate de zinc, le pentaérythritol, etc, Les effets de certains stabilisateurs thermiques sur les propriétés plastifiantes et mécaniques du PVC ont été caractérisés ; enfin, le mécanisme de stabilisation thermique du 2,3⁃LPDA a été étudié.
1
Préparation de l'échantillon
Préparation du 2,3⁃LPDA : peser la quantité appropriée d'oxyde de lanthane dans un bécher, ajouter de l'eau déminéralisée et bien remuer ; mettre le bécher dans le 60 ℃ chauffage du bain d'eau, en remuant la solution aqueuse d'oxyde de lanthane avec un agitateur, puis utiliser le compte-gouttes pour ajouter lentement la solution d'acide nitrique à la solution d'oxyde de lanthane est complètement dissoute ; la valeur du pH de la solution a été déterminée à 3~4 par le papier pH pour la filtration, le filtrat obtenu pour la solution de nitrate de lanthane, et versé dans une bouteille de réactif pour la réserve, et sa valeur molaire était de 0.015 mg/L. La solution a été filtrée puis versée dans un flacon de réactif. La concentration molaire de la solution de réserve a été déterminée par titrage à l'EDTA, en pesant le rapport molaire de 3 :2 2,3 ⁃ PDA et nitrate de lanthane, le premier éthanol anhydre sera 2,3 ⁃ PDA poudre dissoute, puis diluer l'ammoniac pour ajuster le pH à 6 ~ 7, sous agitation constante, la solution de nitrate de lanthane est lentement ajoutée à la solution d'éthanol anhydre de 2,3 ⁃ PDA, puis de l'ammoniaque diluée pour ajuster le pH du système à 6 ~ 7, ce qui donne un précipité blanc, avec un agitateur électrique. Le précipité blanc, agité avec un agitateur électrique pendant 3 h pour rendre le système complètement réactif, et ensuite laissé pour laisser le précipité précipité tout, et ensuite filtré, et ensuite lavé le précipité avec de l'éthanol anhydre pendant plusieurs fois ; le composite a été séché à 50 ℃ à un poids constant, et le produit résultant était 2,3 ⁃ LPDA stabilisateurs de chaleur de terre rare, et puis le produit a été broyé dans une poudre et ensuite emballé dans un sac pour l'utilisation de rechange ;
Préparation du stabilisateur thermique composé : 2,3 ⁃ LPDA avec du stéarate de zinc et du pentaérythritol selon différents rapports de masse du composé binaire et ternaire, pesage, broyage et mélange de la poudre, ensachage de réserve.
2
Résultats et discussion
2.1 Caractérisation du 2,3⁃LPDA
2.1.1 Analyse spectrale infrarouge
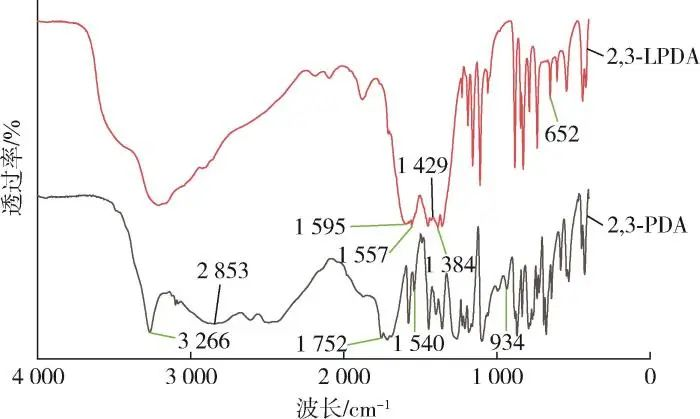
La figure 1 montre les spectres FTIR du 2,3⁃PDA et du 2,3⁃LPDA. On constate que les pics de vibration télescopique de la liaison C=N dans le 2,3⁃PDA et le 2,3⁃LPDA se situent respectivement à 1 540 cm-1 et à 1 557 cm-1 ; les pics de vibration télescopique de NO3- sur le 2,3⁃LPDA se situent à 1 384 cm-1 ; les pics de vibration télescopique de la liaison C=O sur 2,3⁃PDA à 1 752 cm-1 ; les pics de vibration télescopique de la liaison C=O sur 2,3⁃PDA à 1 595 cm-1 et 1 429 cm-1 , respectivement ; les pics de vibration télescopique de 2,3⁃PDA sur 2,3 ⁃PDA à 1 595 cm-1 et 1 429 cm-1 , respectivement. Les pics de vibration télescopique antisymétrique et symétrique de la liaison C=O sur le 2,3⁃LPDA se situent respectivement à 1 595 cm-1 et 1 429 cm-1 ; le pic de vibration télescopique de la liaison O-H sur le 2,3⁃PDA se situe à 3 266 cm-1 ; et le pic caractéristique de -COOH sur le 2,3⁃PDA se situe à 934 cm-1, ce qui nous permet de déterminer que des groupes carboxylates sont présents ; Le pic de vibration d'étirement de la liaison O-La sur le 2,3⁃LPDA à 652 cm-1, indiquant ainsi que la réaction du 2,3⁃PDA avec le nitrate de lanthane comme ligand a provoqué la rupture de la chaîne et la dé-H de la liaison O-H dans le groupe carboxylate du 2,3⁃PDA, et la formation d'une liaison O-La avec l'ion La. En résumé, on peut déterminer que la réaction a produit du 2,3⁃LPDA.
Figure 1 Spectre FTIR de l'échantillon
2.1.2 Analyse élémentaire et thermique
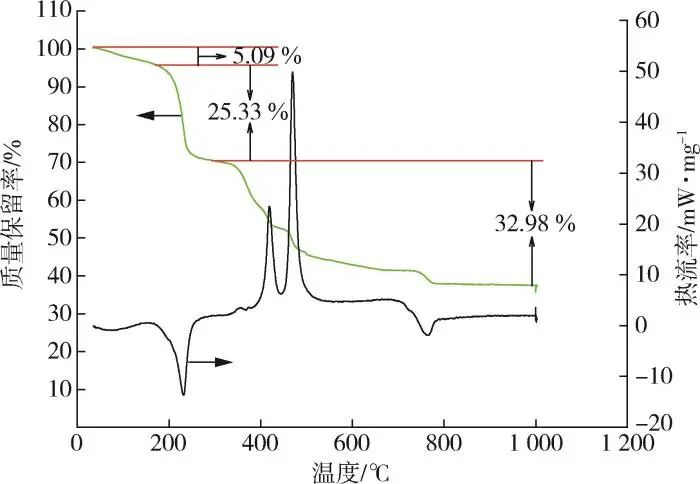
La teneur en éléments C, H et N du 2,3⁃LPDA a été déterminée par analyse élémentaire, et la teneur en lanthane a été déterminée par titrage à l'EDTA. Le tableau 1 montre que l'erreur relative de la teneur en élément H (fraction de masse, voir ci-dessous) est importante en raison de sa faible quantité, et que la teneur réelle des autres éléments est fondamentalement conforme à la teneur théorique. Ensuite, le nombre d'eau de cristallisation a été calculé à partir des résultats de l'analyse thermique de la figure 2, ce qui a conduit à la formule moléculaire du 2,3⁃LPDA comme La2(C6N2O4)2(NO3)2-3H2O. Les courbes TG de la figure 2 montrent que la perte de poids thermique du 2,3⁃LPDA a été divisée en trois phases, à savoir les phases de 50 à 184, 184 à 292 et 292 à 1 000 ℃, respectivement. Le taux de perte de masse de la première étape était de 5,09 %, et à partir du taux de perte de masse, on a déduit qu'il y avait trois eaux cristallines, ce qui était similaire au taux de perte de masse de 6.88 % dans la formule moléculaire La2(C6N2O4)2(NO3)2-3H2O telle que déduite du tableau 1 ; la courbe DSC de la première étape présentait un pic d'absorption de chaleur à 87,1~140,6 ℃, ce qui représentait l'élimination de l'eau cristalline du 2,3 ⁃LPDA. Les courbes TG des deuxième et troisième étapes montrent que le 2,3 ⁃LPDA a subi une perte de poids en falaise, avec une perte de masse totale de 58,31% aux deuxième et troisième étapes ; contrairement aux courbes DSC, un pic d'inspiration de 184~292,4 ℃ est apparu au cours de la deuxième étape, ce qui représente la décomposition du produit. Deux pics exothermiques sont apparus au cours de la troisième étape, représentant la décomposition ultérieure des produits. Après 797 ℃, il n'y a plus de perte de poids, et la courbe TG tend à s'aplatir, et son résidu final est La2O3, qui représente 36,59% de la fraction de masse, et la teneur en La est calculée comme étant de 31,11%, ce qui est similaire à la teneur théorique en La de 31,53% dans le tableau 1. En résumé, la formule moléculaire du stabilisateur thermique à base de terres rares a été déterminée comme étant La2(C6N2O4)2(NO3)2-3H2O en comparant les données du tableau 1 et de la figure 2.
Tableau 1 Résultats de l'analyse élémentaire du 2,3⁃LPDA
Fig. 2 Courbe d'analyse thermique du 2,3⁃LPDA
2.2 Analyse de la stabilité thermique
2.2.1 Stabilisateur thermique simple
Afin d'étudier plus en profondeur la stabilité thermique du 2,3⁃LPDA, sa stabilité thermique a été comparée à celle de stabilisateurs thermiques courants, et les résultats sont présentés dans le tableau 2. Le tableau 2 montre que le temps de stabilisation thermique du 2,3⁃LPDA est de 30 minutes, soit 6 fois plus long que celui du 2,3⁃PDA, seulement plus court que celui du stéarate de plomb, et plus long que celui des autres stabilisateurs thermiques du tableau. En termes de performance anti-décoloration, le 2,3⁃LPDA a une meilleure performance anti-décoloration initiale que le 2,3⁃PDA, ce qui indique que le 2,3⁃LPDA a une capacité de liaison plus forte avec le Cl- instable, et améliore la performance anti-décoloration initiale du PVC. En termes de performance anti-décoloration à long terme, le 2,3⁃LPDA est un peu plus faible que le stéarate de calcium et le pentaérythritol en termes de capacité anti-décoloration. À l'exception du stéarate de calcium et du pentaérythritol, le 2,3⁃LPDA présente certains avantages par rapport à d'autres stabilisateurs thermiques en termes de capacité anti-décoloration, et il a un effet positif sur la prévention de la dégradation thermique du PVC.
Tableau 2 Stabilité thermique de différents stabilisateurs thermiques
2.2.2 2,3⁃LPDA composé de stéarate de zinc
La résistance à la décoloration initiale du 2,3⁃LPDA est légèrement inférieure à celle du stéarate de zinc, mais son temps de stabilisation thermique et sa résistance à la décoloration à long terme sont bien meilleurs que ceux du stéarate de zinc. Les résultats des tests de stabilité thermique des deux complexes sont présentés dans le tableau 3. Le tableau 3 montre que le temps de stabilité thermique le plus long était de 34 minutes lorsque le rapport de mélange de 2,3⁃LPDA et de stéarate de zinc était de 4:1, et qu'il était plus long que lorsque le 2,3⁃LPDA était utilisé comme stabilisateur thermique seul, et que plus la proportion de 2,3⁃LPDA dans le rapport de mélange était importante, plus le temps de stabilité thermique était long. Cela s'explique par le fait que Re3+ et Cl- ont de forts effets de coordination et se coordonnent plus facilement avec Cl- décomposé par la chaleur. En termes de performance anti-décoloration, la performance anti-décoloration initiale des stabilisateurs thermiques composés a été considérablement améliorée. En effet, l'inhibition initiale du stéarate de zinc par le 2,3 ⁃ LPDA pour produire le phénomène de "brûlure du zinc" est évidente, et il y a un fort effet synergique, le mélange de la performance anti-coloration initiale du PVC a été grandement amélioré. Cependant, du point de vue de la performance anti-décoloration à long terme, le 2,3 ⁃ LPDA seul est meilleur que la performance anti-décoloration composée, et le 2,3 ⁃ LPDA dans le rapport de composition de la plus petite proportion, le phénomène de "combustion du zinc" sera plus évident, plus mauvaise sera la performance anti-décoloration à long terme, plus le temps de stabilisation à la chaleur est court, ce qui indique que plus la proportion de stéarate de zinc dans le rapport de mélange est importante, plus la proportion de 2,3 ⁃ LPDA et de stéarate de zinc est importante, et plus la proportion de 2,3 ⁃ LPDA et de stéarate de zinc est importante, plus la proportion de 2,3 ⁃ LPDA et de stéarate de zinc est importante. Plus le temps de stabilisation à la chaleur est court, ce qui indique que plus la proportion de stéarate de zinc est importante dans le rapport de mélange, plus l'effet synergique entre le LPDA et le stéarate de zinc est mauvais.
Tableau 3 Stabilité thermique des systèmes composés de stéarate de zinc
2.2.3 Mélange de 2,3⁃LPDA avec du pentaérythritol
Le pentaérythritol est un stabilisateur thermique auxiliaire doté d'une excellente stabilité thermique, et ses performances anti-décoloration à court et à long terme sont bonnes. La stabilité thermique du 2,3⁃LPDA et du pentaérythritol complexés est indiquée dans le tableau 4. Le tableau montre que le temps de stabilité thermique des deux stabilisateurs thermiques complexés est compris entre 31 et 34 minutes, et que le temps de stabilité thermique du 2,3 ⁃LPDA en tant que stabilisateur thermique seul est de 30 minutes, ce qui indique que le temps de stabilité thermique du 2,3 ⁃LPDA en tant que stabilisateur thermique complexé est de 30 minutes, ce qui indique que le temps de stabilité thermique du 2,3 ⁃LPDA avec du pentaérythritol complexé avec du stéarate de zinc est de 30 min, ce qui indique que l'effet synergique entre le 2,3⁃LPDA et le stéarate de zinc est de plus en plus important. L'effet de stabilisation thermique du mélange de 3⁃LPDA et de pentaérythritol n'est pas évident, le temps de stabilisation thermique n'est prolongé que de 1 à 3 minutes, mais il a également un certain effet synergique. En termes de performance anti-décoloration, l'effet du pentaérythritol est très évident, et la performance anti-décoloration initiale des deux composites est meilleure que celle du 2,3⁃LPDA seul en tant que stabilisateur thermique. En ce qui concerne la performance anti-coloration à long terme, plus la proportion de pentaérythritol dans le stabilisateur thermique composé est importante, meilleure est la capacité anti-coloration à long terme, ce qui indique que le mélange de pentaérythritol et de 2,3⁃LPDA a une bonne performance anti-coloration, et que le pentaérythritol augmente encore la performance anti-coloration à long terme du 2,3⁃LPDA. Dans l'ensemble, l'effet de stabilisation thermique du pentaérythritol n'est pas évident, mais la propriété anti-décoloration est très importante. Ceci est dû à la capacité de l'alcool à modifier la coloration du PVC lorsqu'il est chauffé, et à mesure que la température augmente, l'alcool subit une estérification, ce qui rend plus difficile la précipitation de l'alcool hors du PVC. En même temps, le pentaérythritol et le lanthane peuvent être complexés pour compenser les chaînes brisées dans la chaîne moléculaire lors de la dégradation du PVC, ce qui renforce la capacité de changement de couleur à long terme du PVC.
Tableau 4 Stabilité thermique du système complexe de pentaérythritol
2.2.4 Mélange de 2,3⁃LPDA, de stéarate de zinc et de pentaérythritol
Le phénomène de "brûlure du zinc" causé par le stéarate de zinc peut être retardé par le pentaérythritol. Afin que les stabilisants thermiques aient une capacité de changement de couleur et un temps de stabilisation thermique plus excellents, le 2,3⁃LPDA, le stéarate de zinc et le pentaérythritol ont été composés, et leur stabilité thermique est indiquée dans le tableau 5. Comme le montre le tableau 5, lorsque le rapport 2,3⁃LPDA:stéarate de zinc:pentaérythritol était de 2:1:2, le temps de stabilisation thermique était de 44 minutes, ce qui était supérieur à celui des deux autres ensembles de rapports de mélange, ce qui prouvait pleinement qu'il y avait un fort effet synergique lorsque le 2,3⁃LPDA et le pentaérythritol représentaient la même proportion. Du point de vue de la performance anti-décoloration, l'ajout de pentaérythritol a considérablement amélioré l'anti-décoloration du système composé, et le pentaérythritol a également ralenti l'apparition du phénomène de "brûlures de zinc" du stéarate de zinc, l'anti-décoloration à long terme du système après les trois mélanges a été considérablement améliorée. En comparant le tableau 2, le tableau 3 et le tableau 5, on constate que la performance anti-décoloration du système de mélange ternaire est nettement supérieure à celle du mélange binaire. En effet, dans une certaine mesure, les stabilisateurs thermiques auxiliaires des polyols peuvent empêcher l'apparition du phénomène de "combustion du zinc" du stéarate de zinc, et le complexe généré par la réaction entre le pentaérythritol et le stéarate de zinc peut effectivement affaiblir l'effet catalytique du ZnCl2 sur la dégradation du PVC.
Tableau 5 Stabilité thermique du système de mélange ternaire
2.3 Analyse des propriétés de plastification
Dans cette étude, des expériences de plastification ont été réalisées avec différents stabilisateurs thermiques pour étudier l'effet des stabilisateurs thermiques sur la stabilité thermique dynamique du PVC, et les résultats sont présentés dans le tableau 6. Comme le montre le tableau, le temps de plastification de l'échantillon de stabilisateur thermique contenant du stéarate de zinc composé de 2,3⁃LPDA était le plus long. C'est parce que le stéarate de zinc seul plastifie, la performance de plastification est très faible, à la fin de la charge, apparaîtra immédiatement le phénomène de "brûlure du zinc", le phénomène favorisera la dégradation du PVC, ne peut pas réaliser la plastification ; et avec le complexe 2,3 ⁃ LPDA, 2,3 ⁃ LPDA a joué un rôle dans le ralentissement du phénomène de "brûlure du zinc", l'effet du phénomène de "brûlure du zinc", l'effet du phénomène de "brûlure du zinc". " Après le pic de plastification, le stéarate de zinc a commencé à favoriser la dégradation du PVC, entraînant une décomposition accélérée de la poudre de PVC. Bien que le temps de plastification de l'échantillon contenant le stabilisateur thermique ternaire soit légèrement plus long que celui de l'échantillon contenant le 2,3 ⁃LPDA, son couple de plastification et son couple d'équilibre sont plus faibles, ce qui indique qu'il peut réduire l'adhérence entre le PVC et la machine de traitement pendant le processus, réduisant ainsi la perte d'énergie et la consommation d'énergie.
Tableau 6 Propriétés de plastification des différents échantillons
2.4 Analyse des propriétés de traction
Selon les résultats des expériences de stabilisation thermique statique, les stabilisateurs thermiques à base de terres rares présentant les meilleures performances de stabilisation thermique dans chaque groupe d'expériences ont été sélectionnés pour l'essai de résistance à la traction afin d'étudier l'effet des différents stabilisateurs thermiques sur les propriétés de résistance à la traction du PVC, et les résultats sont présentés dans le tableau 7. Les résultats sont présentés dans le tableau 7. Le tableau montre que les propriétés de traction du PVC ont été significativement améliorées après l'ajout de 2,3⁃LPDA au PVC ; la différence de propriétés de traction entre les échantillons de stabilisateur thermique contenant du 2,3⁃LPDA et du stéarate de zinc et les propriétés de traction des échantillons contenant du 2,3 ⁃LPDA était importante, ce qui peut être dû au fait qu'une partie du stéarate de zinc semblait présenter le phénomène de "zinc brûlé" lors du mélange avec la feuille de PVC, ce qui a favorisé la dégradation du PVC. Cela peut être dû au phénomène de "combustion du zinc" de certains stéarates de zinc lors du mélange des flocons de PVC, qui favorise la dégradation du PVC et réduit la résistance à la traction des flocons de PVC, ce qui se traduit par des propriétés mécaniques médiocres des flocons de PVC. Les dernières données du tableau 7 montrent que le 2,3⁃LPDA, le stéarate de zinc et le pentaérythritol ont le meilleur effet sur l'amélioration de la résistance à la traction du PVC. Cela peut être dû au fait que les éléments des terres rares ont de nombreuses orbitales vides pour accepter l'électron solitaire du ligand, tandis que les ions métalliques des terres rares ont un grand rayon ionique, de sorte qu'ils et les substances organiques et inorganiques dans la formule du PVC pour former une variété de ligands ou de chélates, augmentant la force d'interaction intermoléculaire, le PVC a joué un effet plastifiant, et améliorer la résistance à la traction des matériaux en PVC.
Tableau 7 Propriétés mécaniques des différents échantillons
2.5 Mécanisme de stabilisation thermique
Les spectres FTIR du 2,3⁃LPDA avant et après traitement au HCl sont présentés dans la figure 3. La figure montre que les spectres FTIR du 2,3⁃LPDA après traitement au HCl ont déplacé le nombre d'ondes de la liaison C=N d'un nombre d'ondes faible à un nombre d'ondes élevé par rapport au non-traité, et le nombre d'ondes de la liaison C=N après traitement était de 1 572 cm-1. En outre, le pic de vibration télescopique de NO3- a disparu des courbes après le traitement avec HCl, car le H+ se combine avec NO3- pour former HNO3. Cependant, en raison de la combinaison de H+ et de NO3- pour former HNO3 lors du traitement du 2,3⁃LPDA avec HCl, il n'est pas possible de déterminer le mécanisme de stabilisation thermique du 2,3⁃LPDA. Lors du traitement du 2,3⁃LPDA avec du HCl, la solution de HCl est exothermique, tandis que le HNO3 est facilement décomposé en H2O, NO2 et O2 dans des conditions de haute température, ce qui n'affecte pas les propriétés de stabilité thermique du 2,3⁃LPDA. Dans le spectre FTIR du 2,3⁃LPDA non traité, le pic de vibration d'étirement de la liaison O-La se situe à 652 cm-1. Après traitement, deux autres pics caractéristiques de la liaison O-H sont apparus dans les spectres FTIR, le pic de vibration télescopique de la liaison O-H à 1 445 cm-1 et le pic de vibration télescopique hors plan de la liaison O-H à 1 097 cm-1, et les spectres sont réapparus avec le pic caractéristique de la liaison - COOH. On peut déduire de ce qui précède que la liaison O-La a été rompue et que la liaison O-H a été recombinée après le traitement, et qu'après la rupture de la liaison O-La, les ions La se sont combinés avec les ions Cl pour former la liaison La-Cl, et d'après les spectres FTIR du 2,3 ⁃LPDA traité, un pic supplémentaire à 1 261 cm-1 a été trouvé dans les spectres FTIR du 2,3 ⁃LPDA. Le spectre FTIR du 2,3⁃LPDA après traitement présente un pic de 1 261 cm-1 , qui est le pic de vibration d'étirement de la liaison La ⁃Cl. On peut voir que le 2,3⁃LPDA a réagi avec HCl pour former LaCl3, ce qui permet de savoir que le mécanisme de stabilisation du 2,3⁃LPDA est que le 2,3⁃LPDA peut absorber efficacement le gaz HCl libéré pendant la dégradation thermique du PVC et former LaCl3, ce qui peut retarder l'effet catalytique de la dégradation thermique du PVC jusqu'à un certain point.