영문명】에틸 비닐 에테르
분자식] [분자식 C4H8O
분자량】72.11
CAS 등록 번호][109-92-2]
구조식】CH3CH2OCH=CH2
[물리적 특성] bp 33 oC, d 0.753 g/cm3. 대부분의 유기 용매에 용해되며 다양한 유기 용매에 사용할 수 있습니다.
[조제 및 상품] 이 시약은 국내외 화학 시약 회사에서 판매되고 있습니다.
[주의] 이 시약은 휘발성이 높고 인화성이 강한 화학물질입니다. 저온의 건조한 곳에 보관하고 흄 후드에서 사용하는 것이 좋습니다.
에틸 비닐 에테르는 주로 수산기의 보호기, 비닐 전이 시약으로 사용되며 유기 합성에서 고리화 첨가 반응에 참여합니다.
하이드 록시 그룹의 많은 보호기 중에서 에틸 비닐 에테르와 하이드 록시에 의해 형성된 α- 에톡시 에틸 에테르 (EE)는 가장 일반적으로 사용되고 편리한 보호기 중 하나입니다. 반응에는 일반적으로 강산 촉매가 필요하며, 이를 위해 TFA와 TsOH를 사용할 수 있으며, 가장 일반적으로 사용되는 것은 PPTS입니다. 반응은 일반적으로 실온에서 몇 시간 동안 저어주면 완료됩니다. 대부분의 경우, 생성물의 수율은 95%(공식 1) 이상입니다[1,2]. EE 보호 그룹은 산성 조건에서 쉽게 탈보호 반응을 완료할 수 있습니다. PPTS-EtOH 및 aq. HCl-MeOH가 권장되는 방법입니다(공식 2).

수은 아세테이트 유도체 촉매의 작용으로 에틸 비닐 에테르와 하이드 록실은 비닐 전이 반응을 거쳐 해당 비닐 에테르 생성물을 생성합니다 (공식 3) [5]. 금속 팔라듐 촉매를 사용하면 금속 수은 촉매의 사용을 효과적으로 피할 수 있습니다(공식 4)[6]. 이 반응은 생성물이 추가 축합 반응 또는 올레핀 메타테스를 겪을 수 있기 때문에 더욱 의미가 있습니다 [7,8].
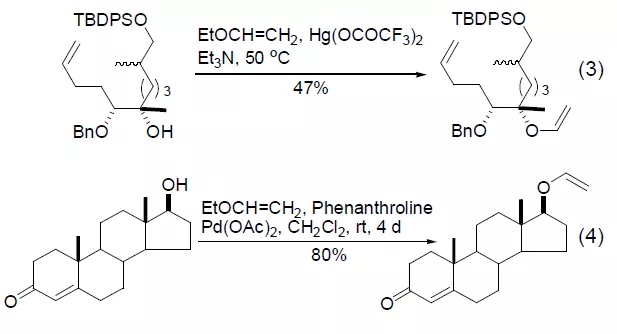
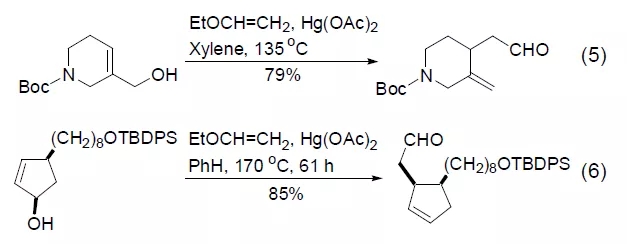
에틸 비닐 에테르와 알릴 하이드 록실은 비닐 전이 반응을 거쳐 해당 비닐 에테르 생성물을 생성합니다. 이 반응은 일반적으로 아세트산 수은의 촉매 작용으로 완료됩니다. 톨루엔 또는 자일렌에서 생성물을 가열하면 해당 클라이젠 재배열을 유도하여 중요한 합성 가치의 반응을 일으킬 수 있습니다. 정상적인 상황에서 2단계 반응 과정은 "원팟 요리"(방정식 5, 방정식 6) 조건에서 완료될 수 있습니다[9~11].
루이스 산 촉매가 있는 경우, 에틸 비닐 에테르도 해당 고리화 반응을 거칠 수 있습니다 [12,13].
