Széles körű alkalmazása miatt a kereslet a allantoin évről évre növekszik . Az allantoin kémiai szintézisének módszere az 1940-es években jelent meg külföldön. De csak az 1970-es évek végén és az 1980-as évek elején Japánban és Nyugat-Németországban vezették be az ipari termelésbe. A hazai allantoinszintézis fejlesztése viszonylag későn kezdődött, a kutatás és fejlesztés az 1970-es évek végén kezdődött. Jelenleg csak néhány hazai vállalat ért el kísérleti vagy tömeggyártást . Mivel kevés gyártó van, a piac rendkívül szűkös. Az allantoin különleges fizikai és kémiai tulajdonságai miatt az allantoin-származékok sokfélék és széles körben használatosak. Napjainkig az allantoin és származékai még mindig tovább küldik a fejlődést.
Quick answer: A practical additive decision starts with the exact defect: foam, poor wetting, craters, haze, or instability. The best product is usually the one that solves that defect with the safest compatibility window.
Allantoin, kémiai neve 1-urea-m-diazocén - [2,4]; Acetaldehid Tetraaza ciklopentadién; (2,5-dioxocén-4-m-diazopentil) karbamid; 5-urea hidantoin stb. Az imidazol heterociklusos vegyületek közé tartozik, molekuláris képlete C4H6N4O3molekulatömege 158,12 g/mol. Az allantoin kristály vagy kristályos por, amelynek színe színtelen és fehér között van, és szagtalan és íztelen. Az allantoin olvadáspontja 220 ~ 238 ℃. Az allantoin vízben, alkoholban, éterben és kloroformban nem oldódik, forró vízben, híg etanolban és propan-triolokban oldódik. A telített vizes oldat (0,6%) enyhén savas volt, pH =. 6. A vizes oldatban a pH = 4-9, stabil marad, és egy nem vizes oldószer és szárító levegőn stabil , még a 80 ~ 90 ℃ 30 perc alatt hő alatt is változatlan maradt.
De nem bírja a magas hőmérsékletet (100 ℃ felett), az erős bázist, vagy a hosszú ideig tartó forralást és a napfényt. Az allantoin izomerekkel rendelkezik, és a szerkezeti képlet a következő:

Az alkoholkonjugált rendszer az oka a savas csoportok kialakulásának, és stabilizálhatja a molekulákat. Az OH– egyesek azt gondolhatják, hogy az allantoin egy bináris savas vegyület. Általánosságban azonban a C(4)-en lévő hidrogénnek nagyon alacsony az aktivitása és gyenge a disszociációs állandója. A szén (2) helyén lévő sav erősebb, és a disszociációs állandója 1,17 × 10-9. Ezért a sóknak csak egyetlen sorozata, savas sók vagy bázikus sók képződhetnek. Ezért az allantoin monobázisos sav-bázis amfoter vegyület. Létezhet alkoholos és ketonos forma is. Mint amfoter vegyület, az allantoin nemcsak bázikus vegyület, hanem gyenge sav is, és a savas sóvegyületekhez gyenge bázis is. Ezért az allantoin számos anyaggal képes fémsókat és adduktokat képezni. Ezek a fémsók és adduktok nem csak magának az allantoinnak a tulajdonságait tartják meg, hanem nem veszítik el a hozzáadott anyagok inherens tulajdonságait sem. A következőkben példaként felsoroljuk az allantoin alumíniumvegyületek néhány fizikai és kémiai tulajdonságát.
Az allantoin alumíniumvegyületek a bőrbetegségek kezelésében hatékony funkciók széles skáláját biztosítják. Mivel az alumíniumion és az allantoin ideális tulajdonságainak konvergenciája teljes mértékben egyesül. Az allantoin jelenléte javítja az alumíniumsó hatását, és megszünteti az alumíniumsó-allergiában szenvedő egyes betegek irritációját. Állatkísérletek azt is kimutatták, hogy az allantoin alumínium só nem volt irritáció és allergia. Számos gyakori formája a következő:
1. Alumínium-dihidroxi allantoinát
Az alumínium-dihidroxiallantoinát molekuláris képlete Al(OH)2C4H5N4O3. Fehér por, vízben és más oldószerekben, például etanolban, éterben és kloroformban nem oldódik. Nemzetközi kereskedelmi neve "aldioxa".Az alumínium-dihidroxi allantoinát összetétele a következő: alumínium-oxid (22,0 ± 5)%, allantoin (55,0 ± 5)%, pH-értéke (4% szuszpenzió) 6-5,8.
2. Alumínium klórhidroxi-allantoinát prorilénglikol
Az alumínium-dihidroxiallantoinát molekuláris képlete [Al2(OH)4ClC4H5N4O3]C3H8O2. Ez egy fehér por, molekuláris állapotban vagy módosított formában, és dezodorként, nedvesítőszerként és bőrösszehúzó szerként használják.
3. Alumínium-klór-droxi allantoinát
Az alumínium-klór-hidroxi allantoinát képlete: Al2(OH)4ClC4H5N4O3. Az alumínium-klór-hidroxi allantoinát tiszta fehér por, vízben oldódik, etanolban enyhén oldódik, éterben és klórutánzatban nem oldódik. Az alumínium-klór-hidroxi allantoinát nemzetközi kereskedelmi neve "alcloxa".Az összetétel a következő: Alumínium-oxid (28,0 ± 3)%, allantoin (40,0 ± 3)%, klór (9,5 ± 1,5)%, nitrogén (14,2 ± 1,5)%.
Ugyanakkor a módosított klór-alumínium-allantoin összetétele a következő : Alumínium-oxid (45,61 ± 2,0)%, allantoin (1,25 ± 0,3)%, klór (15,60 ± 1,5). Az alumínium-klór-hidroxi allantoinát 10% oldatának pH-értéke körülbelül 4,3 .
Az irodalmi jelentések szerint az allantoin fő szintetikus módszerei a következők:
1. Húgysav reakciója kálium-permanganáttal
A húgysavat és a kálium-permanganátot lúgos közegben oxidálják, és a termékeket ecetsavval dekarboxilálják. Az oxidálószerek lehetnek ólom-dioxid, kálium-ferricyanid, oxigén, ózon, mangán-dioxid, hidrogén-peroxid stb. is. A reakció folyamata a következő:
Először is, oxidációs reakció. A húgysav és a kálium-permanganát reakcióba lép.
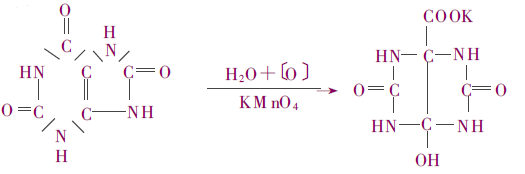
Ezután dekarboxilációs gyűrűnyitási reakcióval kapjuk a végterméket.
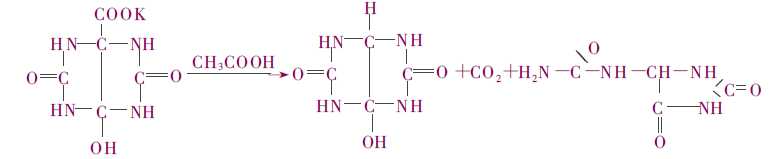
Ez a legkorábbi eljárás, amely a nyersanyaghiány, a magas ár, a nagy mennyiségű berendezés és a magas költségek miatt csak kis tételes gyártásra korlátozódik.
2. Lítium-urát elektrolitikus oxidációja
Az allantoint glikolsav és karbamid elektromos áram alatt történő kondenzációjával szintetizálták.
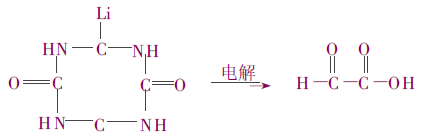
Bár ennek a módszernek a hozama valamivel magasabb, mint a húgysav-oxidációs módszeré, a fenti problémákkal is küzd, és kevésbé alkalmazható iparilag.
3. Oxálsav elektrolitikus oxidációja
Ez egy új, az elmúlt években kifejlesztett eljárás, és ez a gyártósor Kínában jött létre. A nyersanyagok könnyen beszerezhetők, de az energiafogyasztás nagy. A szakirodalom szerint az eljárás nem kiforrott, és fejlesztésre szorul.
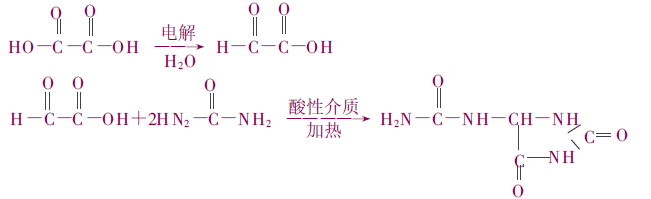
4. A glioxál oxidációja
Mivel a glioxál részleges oxidációjával előállítható a glioxilsav, és az eljárás körülményei enyhék, ezt a szintetikus utat gyakran használják az iparban. Ez a módszer azonban salétromsavat használ az oxidációhoz, ami súlyos környezetszennyezést okoz.
Először a glikoxal részleges oxidációja glikoxilsav előállításához.
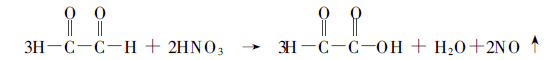
Két mellékreakciót ad az alábbiakban, így a glikolsav előállításának ezen módja kb. 83%.
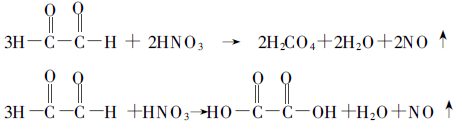
Ezután az allantoin szintézise glikoxilsav és karbamid kondenzációjával, melegítés és savas körülmények között.
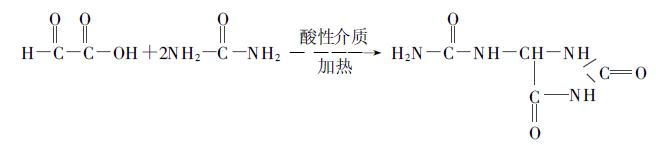
A glikolsav ilyen módon történő átalakulása 52% ~ 58%. Az összes reakció szerint, a glioxálra számolva, az allantoin hozam 38% - 40% az elméleti értékből.
5. Karbamid reakciója diklórecetsavval
2 mol karbamid és 1 mol diklór-ecetsav hevítésével állítják elő. A reakció folyamata a következő:
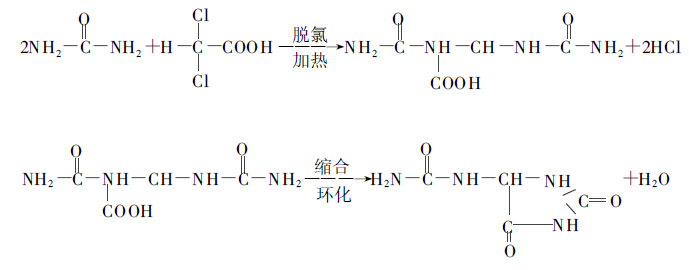
Az 1930-as években egy amerikai szabadalom arról számolt be, hogy az allantoin etilénglikolban 120 ℃-on 4 órán keresztül előállítható, de a hozam alacsony volt. Az allantoin-p-diklórecetsav teljes hozama elérheti a 30,3%-t. Néhány kínai kutató tanulmányozta az eljárást, és az allantoin összhozama meghaladta a 40%-t. A teljes rutin a következő.
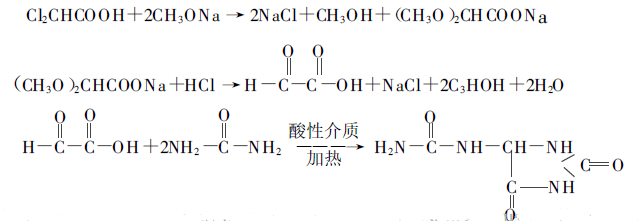
Jelenleg a technológiafejlesztés és a kutatás más módszerei is nagyon aktívak, és megpróbálnak alacsonyabb költséggel sikereket elérni, mint például az acetilén módszer, a szén-dioxid, a szén-monoxid és más, magas tartalmú hulladékgáz-hasznosítási módszerek. Eddig azonban még nem került sor a termelésbe való bevezetésre. Fontos ipari termékként az allantoin további szintetikus kutatásokat igényel.
hol lehet megvásárolni Allantoin?
A Longchang Chemical az Allantoin CAS 97-59-6 gyártására és szállítására specializálódott. Általában 24 órán belül felvesszük Önnel a kapcsolatot. A munkaidőben ( 8:30-18:00 UTC+8 H.~Szombat ) vagy a weboldal élő chat segítségével a info@longchangchemical.com e-mail címre is küldhet e-mailt, hogy azonnali választ kapjon.
Ezt a cikket a Longchang Chemical R&D Department írta. Ha másolni és újranyomtatni szeretné, kérjük, adja meg a forrást..
A practical selection checklist for wetting, leveling, and defoaming additives
Additive selection is usually most effective when the team defines the defect first and then screens compatibility, dosage range, and process stage. That is often much more reliable than choosing only by chemistry family or by a single dramatic lab result.
- Start from the defect, not the additive name: wetting loss, crater, microfoam, and instability often need different solutions even inside the same formula.
- Check compatibility at the intended dosage: the strongest additive can still be the wrong commercial choice if it narrows the process window too much.
- Review the stage of use: some products are most useful during grind, while others matter more during let-down, filling, or final application.
- Balance cure or film quality with defect control: the right additive fixes the problem without sacrificing adhesion, gloss, or appearance.
Recommended product references
- CHLUMIAF 094: A balanced defoamer reference for waterborne coatings and many general foam-control screens.
- CHLUMIAF 3062: Useful when printing-ink and UV-ink compatibility matter in the defoaming screen.
- CHLUMIAF 3037: A stronger process-defoaming option when persistent foam survives harsher conditions.
- CHLUMIWE 3280: A strong wetting-agent reference for inks, coatings, and difficult substrate wetting.
FAQ for buyers and formulators
Why does an additive that looks powerful in a beaker sometimes fail in production?
Because shear, temperature, substrate, and the full formula can all change the way the additive performs under real process conditions.
Should the most aggressive additive always be preferred?
Not usually. The best additive is the one that solves the real defect while preserving the broadest safe operating window.
