A mágneses biopolimer mikrogömbök olyan új kompozit anyagok, amelyek biológiai anyagokat és szervetlen mágneses anyagokat egyesítenek, hogy mágnesesen érzékeny és biológiailag aktív mikrogömböket alkossanak. Tulajdonságai a szervetlen mágneses anyagoktól, a biológiai anyagoktól és kölcsönhatásaik módszerétől függnek. Jelenleg a legszélesebb körben használt és vizsgált mágneses anyag a Fe3O4 mágneses nanorészecskék. Nagy fajlagos felületének, jó biokompatibilitásának és magas mágneses válaszának köszönhetően gyors elválasztást és célzott mozgást tud elérni, így széles körben alkalmazható az élelmiszer- és orvosi ellátásban, a környezetvédelemben és más területeken. A biopolimer anyagok közé tartozik elsősorban a kitozán, a nátrium-alginát, a zselatin stb. Közülük a kitozán a leginkább vizsgált biológiai anyag a jó biokompatibilitás, a megújuló erőforrások és a biológiai lebonthatóság saját jellemzői miatt. A kitozánból és mágneses anyagból álló új típusú kompozit anyag mindkettő kiváló tulajdonságokkal rendelkezik, így széleskörű alkalmazási lehetőségekkel rendelkezik különböző területeken.

1. Mágneses biopolimer mikrogömbök szerkezete és tulajdonságai

A mágneses biopolimer mikrogömbök szerkezete háromféle lehet: (1) mag-héj szerkezet; (2) hibrid szerkezet; (3) többrétegű szendvicsszerkezet, amint azt az 1. ábra mutatja.
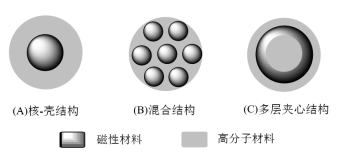
1. ábra A mágneses biopolimer mikrogömbök szerkezete

A mágneses biopolimer mikrogömbök számos kiemelkedő tulajdonsággal rendelkeznek, ami alkalmassá teszi őket az enzimek immobilizálására. Ilyen például (1) a felületi hatás. Általában, amikor a mágneses biopolimer mikrogömbök részecskemérete eléri a mikron vagy akár a nanométeres szintet, a fajlagos felület növekedésével a mikrogömbök csoportsűrűsége és szelektív adszorpciós teljesítménye is nő, és a mikrogömbök stabilitása jelentősen megnő. (2) Mágneses hatás. Amikor a Fe3O4 kristály kisebb, mint 30 nm, szuperparamágnesességgel rendelkezik, azaz külső mágneses tér hatására nagyon nagy a mágnesesség. Amikor a külső mágneses mezőt eltávolítják, mágnesessége gyorsan eltűnik, így a mikrogömb külső mágneses tér állapotában mágneses orientációval rendelkezik, és képes gyorsan elválni a nem mágneses anyagoktól, és mágneses térben nem mágneseződik tartósan, így nem befolyásolja a későbbi felhasználást. (3) Biokompatibilitás. A természetben a biológiai anyagok, például a fehérjék és a poliszacharidok biokompatibilitással rendelkeznek, ami miatt fontos alkalmazásokkal rendelkeznek az orvosbiológiai technikában. (4) Funkcionális alapjellemzők. Az olyan biológiai anyagok, mint a kitozán és a nátrium-alginát, bőségesen rendelkeznek aktív csoportokkal (-OH, -COOH, -NH2), amelyek kovalensen összekapcsolhatók biológiailag aktív anyagokkal, vagy bizonyos kémiai csoportokkal módosíthatók.

2. Mágneses biopolimer mikrogömbök előállítása

A mágneses biopolimer mikrogömbök előállítása két lépésre oszlik. Az első lépés a mágneses nanorészecskék előállítása. A jelenleg használt módszerek a Fe3O4 A mágneses nanorészecskék előállítása elsősorban a kémiai ko-leválasztás, a vas-só termikus bomlása, a mikroemulzió és a hidrotermikus módszerek közé tartozik. Ezek közül a kémiai ko-precipitációs módszer egyszerű és kényelmesen működtethető, és ez a leggyakrabban alkalmazott előállítási módszer. A kémiai ko-leválasztási módszer elve a Fe3O4 a vas-oxid szintetizálása egy bizonyos arányú Fe2+ és Fe3+ (1:2) anaerob körülmények között, majd gyorsan lúgot (ammónia vagy NaOH) adunk hozzá. Xu és munkatársai a kémiai ko-precipitációs módszert alkalmazták 4,34 mmol FeCl2鑘4H2O és 8,67 mmol FeCl3-6H2O, és a rendszert 85 ℃-ra melegítjük nitrogén alatt. Miután teljesen feloldódott, gyorsan adjunk hozzá 25 ml tömény ammóniát és adjunk hozzá bizonyos mennyiségű nátrium-citrátot, majd a Fe3O4 mágneses nanorészecskéket szintetizálnak jó monodiszperzitással és mágneses érzékenységgel.

A mágneses nanorészecskék előállítása után a mágneses kitozán mikrogömbök előállítása érdekében keresztkötést kell végezni kitozánnal. Jelenleg a mágneses kitozán mikrogömbök szintézisének módszerei főként az emulziós térhálósítási módszer, a permetszárítási módszer, a fotokémiai módszer és az in-situ módszer. Ezek közül az emulziós térhálósító módszer az egyszerűbb és a legszélesebb körben használt. Az emulziós térhálósító módszer a Fe3O4 vagy mágneses folyadékot egy kevert folyadékban, amely kitozánt, felületaktív anyagot és olajfázist tartalmaz, hogy víz az olajban mikroemulziós rendszert képezzen, majd adjunk hozzá glutaraldehidet, a rendszerben a glutaraldehid és a kitozán között keresztkötési reakció megy végbe, hogy egy Schiff-bázist hozzon létre, és a kitozán hálózatba kapcsolódik, majd bevonja a Feats-eket.3O4 (amint az a 2. ábrán látható). Jiang és munkatársai emulziós térhálósítási módszert alkalmaztak, Span 80, folyékony paraffin és glutaraldehid mint felületaktív anyag, diszpergálószer és térhálósítószer felhasználásával, szabályos gömb alakú és sima felületű mágneses kitozán mikrogömbök szintézisére.
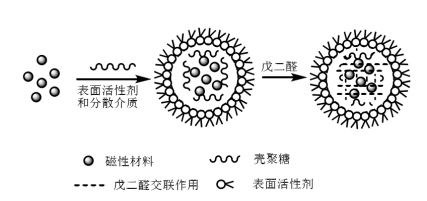
2. ábra Mágneses kitozán mikrogömbök szintézisének vázlata emulziós térhálósító módszerrel

3. Mágneses kompozit mikrogömbökön immobilizált enzim

A mágneses kitozán mikrogömbök sikeres előállítása után az enzim felhasználás céljából immobilizálható a mikrogömbökön. Mivel a kitozán aktív aminocsoportokban és hidroxilcsoportokban gazdag, képes reagálni karboxilcsoportokkal, aminocsoportokkal, epoxicsoportokkal, bifunkciós csoportokkal stb. A mágneses kitozán mikrogömbök csoportmódosítással vannak ellátva, hogy megfeleljenek a különböző immobilizációs igényeknek. A specifikus immobilizált enzimek előállítási módszereit az alábbiakban funkcionális csoportok szerint mutatjuk be.

1) Karboxil módosított mágneses kompozit mikrogömbökön immobilizált enzim
A karboxil-módosított mágneses kompozit mikrogömbök kovalensen kötődhetnek az enzim aminocsoportjához, miután vizes oldatban karbodiimid-kapcsolással aktiválták őket, ezáltal immobilizálva az enzimmolekulát a mágneses kompozit mikrogömbökön (3. ábra). Zhu Yihua és mások egy továbbfejlesztett szuszpenziós polimerizációs módszert alkalmaztak a sztirolnal kezelt mágneses folyadék és a metil-akrilát monomer kopolimerizációjára a térhálósító monomer divinilbenzol segítségével, majd alkáli hidrolízist alkalmazva jó monodiszperzitású és gazdag karboxilcsoportokkal rendelkező mágneses kompozitot kaptak. A mikrogömböket a laktáz immobilizálására használják, miután karbodiimid-kapcsolással aktiválták. A legnagyobb aktivitás körülbelül 360 U-g-1, és az enzim keresztkötési hatékonysága körülbelül 20%.
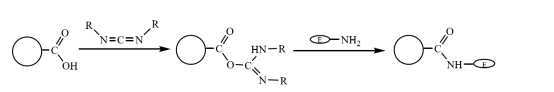
3. ábra A karboxil módosított mágneses kompozit mikrogömbökön immobilizált enzim előállításának sematikus ábrája

2) Aminóval módosított mágneses kompozit mikrogömbök immobilizált enzimmel
Miután az amino-módosított mágneses kompozit mikrogömböket megfelelő mennyiségű glutaraldehiddel összekapcsolták és aktiválták, azok kovalensen kötődhetnek az enzim aminocsoportjához, ezáltal immobilizálva az enzimmolekulákat a mágneses mikrogömbökön (4. ábra). Liu Yu és munkatársai egymás után állítottak elő monodiszperz mágneses SiO2 részecskéket kémiai ko-precipitációs módszerrel és szol-gél módszerrel, aminocsoportokkal módosítottuk őket szilán-kapcsolószerrel, és a laccázt glutaraldehiddel mint térhálósítószerrel immobilizáltuk. Az eredmények azt mutatták, hogy az immobilizált laccáz 4 órán keresztül 60 ℃ állandó hőmérsékleten tartották, és még mindig 60,9% enzimaktivitással rendelkezett, és 10 ciklusos használat után még mindig több mint 55% enzimaktivitással rendelkezett, és hőstabilitása és működési stabilitása nyilvánvalóan javult.
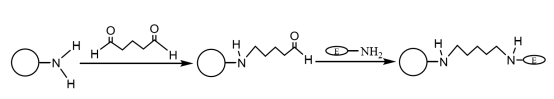
4. ábra Az amino-módosított mágneses kompozit mikrogömbökön immobilizált enzim előállításának sematikus ábrája
3) Epoxi módosított mágneses kompozit mikrogömbök immobilizált enzimmel
Az epoxi csoport egy rendkívül aktív csoport. Közvetlenül, módosítás nélkül kovalens módon biológiai csoportokhoz köthető. Ezért miután az epoxival módosított mágneses kompozit mikrogömbök kovalensen kötődnek az enzim aminocsoportjához az enzim megkötése érdekében, a molekulák immobilizálódnak a mágneses mikrogömbökön (5. ábra). Yong és munkatársai olajsavval bevont mágneses mikrogömböket állítottak elő szuszpenziós polimerizációval. A metanolos aktiválás után kapott hidrofil epoxi alapú mágneses mikrogömböket használták a lipáz immobilizálására. Az immobilizált enzimaktivitás visszatartási aránya 64,2%, és a stabilitása jelentősen javult.
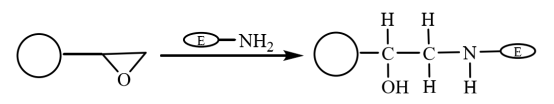
5. ábra Az epoxi alapú mágneses kompozit mikrogömbökön immobilizált enzim előállításának sematikus ábrája

4) Bifunkciós csoportokkal módosított mágneses kompozit mikrogömbökön immobilizált enzimek

A bifunkcionális mágneses mikrogömbökön először az enzimmolekula karboxilcsoportjai és a mikrogömbök aminocsoportjai ionkölcsönhatás révén gyorsan immobilizálódnak a hordozón, és az ionkölcsönhatás révén immobilizált enzim szulfhidril- és aminocsoportjain keresztül kovalens kölcsönhatásba lép a hordozón lévő epoxicsoportokkal. Tegye azt tovább fixálttá (amint az a 6. ábrán látható), amelynek kettős jellemzője van: gyors fixálás ionhatás révén és szilárd fixálás kovalens kötés révén. Li Xiutao és munkatársai három véletlenszerű kopolimer ecsetet vezettek be a divinil-benzollal térhálósított poliakrilsav mikrogömbök felületére Fe3O4 nanorészecskékkel diszpergálták, majd a penicillin G aciláz immobilizálására használták. Az eredmények azt mutatják, hogy az egyszerre epoxi csoportot és aminocsoportot is tartalmazó immobilizált enzim aktivitása és az enzimaktivitás visszanyerési aránya a legmagasabb, immobilizációs kinetikája jobb, mint a csak epoxit tartalmazó mágneses mikrogömböké, és optimális pH-értéke és hőmérsékleti stabilitása magasabb, mint a szabad enzimé, és az enzimaktivitás megtartja a 70%-t 10 alkalommal történő ismételt használat után.
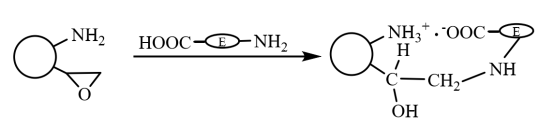
6. ábra A bifunkciós csoportokkal módosított mágneses kompozit mikrogömbökön immobilizált enzim előállításának sematikus ábrája

Az elmúlt években, bár a tudósok különböző anyagokat használtak a naringináz immobilizálására, például természetes biopolimer anyagokat, mint például kitozán, nátrium-alginát és selyemfehérje, szerves vegyületek, mint például epoxigyanta és polivinil-alkohol, aktív szén és grafit-oxid szén anyagok, mint például ene, és bizonyos kutatási eredményeket kaptak, de a tényleges debittering alkalmazásokban vannak problémák, mint például az immobilizált enzimek gyenge savállósága, lassú elválasztás a gyümölcslétől vagy hiányos elválasztás stb. A fenti problémákkal kapcsolatban a következő cikk részletesen bemutat egy kutatási munkát. Ebben a wokban a kutatók egy olyan kompozit anyagot használtak, amelyet kitozán, mágneses Fe3O4 nanorészecskéket és szilícium-dioxidot, és a kompozit anyagot epoxi csoportokkal módosították, majd a naringinázt immobilizálták rajta. Ez a munka adatalapot szolgáltat a naringináz immobilizációs technológiai kutatások további tanulmányozásához.
Lépjen kapcsolatba velünk most!
Ha szüksége van Price-ra, kérjük, töltse ki elérhetőségét az alábbi űrlapon, általában 24 órán belül felvesszük Önnel a kapcsolatot. Ön is küldhet nekem e-mailt info@longchangchemical.com munkaidőben ( 8:30-18:00 UTC+8 H.-Szombat ) vagy használja a weboldal élő chatjét, hogy azonnali választ kapjon.
| Összetétel Glükoamiláz | 9032-08-0 |
| Pullulanase | 9075-68-7 |
| Xilanáz | 37278-89-0 |
| Celluláz | 9012-54-8 |
| Naringináz | 9068-31-9 |
| β-Amiláz | 9000-91-3 |
| Glükóz-oxidáz | 9001-37-0 |
| alfa-amiláz | 9000-90-2 |
| Pektináz | 9032-75-1 |
| Peroxidáz | 9003-99-0 |
| Lipáz | 9001-62-1 |
| Kataláz | 9001-05-2 |
| TANNASE | 9025-71-2 |
| Elasztáz | 39445-21-1 |
| Ureáz | 9002-13-5 |
| DEXTRANASE | 9025-70-1 |
| L-laktil-dehidrogenáz | 9001-60-9 |
| Dehidrogenáz malát | 9001-64-3 |
| Koleszterin-oxidáz | 9028-76-6 |
