En raison de sa large application, la demande de allantoïne augmente d'année en année. La méthode de synthèse chimique de l'allantoïne est apparue dans les pays étrangers dans les années 1940. Mais ce n'est qu'à la fin des années 70 et au début des années 80 que le Japon et l'Allemagne de l'Ouest l'ont mise en production industrielle. Le développement de la synthèse de l'allantoïne dans le pays a commencé relativement tard, et la recherche et le développement ont débuté à la fin des années 1970. À l'heure actuelle, seules quelques entreprises nationales sont parvenues à une production pilote ou de masse. En raison de la rareté des fabricants, le marché est extrêmement étroit. En raison des propriétés physiques et chimiques particulières de l'allantoïne, les dérivés de l'allantoïne sont très variés et largement utilisés. Jusqu'à aujourd'hui, l'allantoïne et ses dérivés continuent à se développer.
Quick answer: A practical additive decision starts with the exact defect: foam, poor wetting, craters, haze, or instability. The best product is usually the one that solves that defect with the safest compatibility window.
AllantoïneLe nom chimique est 1-urea-m-diazocene - [2,4] ; Acetaldehyde Tetraaza cyclopentadiene ; (2,5-dioxocene-4-m-diazopentyl) urea ; 5-urea hydantoin etc. Il s'agit d'un composé hétérocyclique imidazole, dont la formule moléculaire est C4H6N4O3Le poids moléculaire de l'allantoïne est de 158,12 g/mol. L'allantoïne est un cristal ou une poudre cristalline dont la couleur varie entre l'incolore et le blanc, et qui est inodore et sans saveur. Le point de fusion de l'allantoïne se situe entre 220 et 238 ℃. L'allantoïne est insoluble dans l'eau, l'alcool, l'éther et le chloroforme, soluble dans l'eau chaude, l'éthanol dilué et les propan-triols. La solution aqueuse saturée (0,6%) est légèrement acide, pH = 6. Dans une solution aqueuse de pH = 4 à 9, il reste stable, et dans un solvant non aqueux et l'air de séchage est stable, même dans le 80 ~ 90 ℃ 30 min sous la chaleur est également restée inchangée.
Mais elle ne peut pas résister à des températures élevées (supérieures à 100 ℃), à une base forte, ou à une longue période d'ébullition et de lumière du soleil. L'allantoïne possède des isomères, et sa formule structurelle est la suivante :

Le système conjugué d'alcool est à l'origine de la formation de groupes acides et peut stabiliser les molécules. L'existence de OH– peut amener certaines personnes à penser que l'allantoïne est un composé acide binaire. Cependant, d'une manière générale, l'hydrogène en C(4) a une très faible activité et une faible constante de dissociation. L'acide en position de carbone (2) est plus fort et sa constante de dissociation est de 1,17 × 10-9. Par conséquent, une seule série de sels, sels acides ou sels basiques, peut être formée. L'allantoïne est donc un composé amphotère acide-base monobasique. Les formes alcool et cétone peuvent exister. En tant que composé amphotère, l'allantoïne est non seulement un composé basique, mais aussi un acide faible et une base faible pour les composés de sels d'acide. Par conséquent, l'allantoïne peut former des sels métalliques et des adduits avec de nombreuses substances. Ces sels métalliques et ces adduits conservent non seulement les propriétés de l'allantoïne elle-même, mais aussi les propriétés inhérentes aux substances ajoutées. Nous énumérerons ensuite quelques propriétés physiques et chimiques des composés d'aluminium de l'allantoïne à titre d'exemple.
Les composés d'aluminium de l'allantoïne offrent un large éventail de fonctions efficaces pour le traitement des maladies de la peau. La convergence de l'ion aluminium et les caractéristiques idéales de l'allantoïne sont en effet parfaitement combinées. La présence d'allantoïne améliore l'effet du sel d'aluminium et élimine l'irritation de certains patients allergiques au sel d'aluminium. Des expériences sur les animaux ont également montré que l'allantoïne et le sel d'aluminium ne provoquaient ni irritation ni allergie. Les formes les plus courantes sont les suivantes :
1. Dihydroxy allantoïne d'aluminium
La formule moléculaire de l'allantoïne dihydroxy d'aluminium est Al(OH)2C4H5N4O3. Il s'agit d'une poudre blanche, insoluble dans l'eau et dans d'autres solvants, tels que l'éthanol, l'éther et le chloroforme. La composition de l'Alluminum dihydroxy allantoinate est la suivante : oxyde d'aluminium (22,0 ± 5)%, allantoïne (55,0 ± 5)%, pH (suspension de 4%) de 6 à 5,8.
2. Chlo rhydroxy allantoinate d'aluminium prorylène glycol
La formule moléculaire de l'allantoïne dihydroxy d'aluminium est [Al2(OH)4ClC4H5N4O3]C3H8O2. Il s'agit d'une poudre blanche, à l'état moléculaire ou sous forme modifiée, utilisée comme déodorant, agent mouillant et astringent pour la peau.
3. Chlorhy dro xy allantoinate d'aluminium
La formule de l'allantoïne chlorhydrique d'aluminium est Al2(OH)4ClC4H5N4O3. L'allantoinate de chlorhy dro xy d'aluminium est une poudre blanche pure, soluble dans l'eau, légèrement soluble dans l'éthanol, insoluble dans l'éther et l'imitation de chlore. Le nom commercial international de l'allantoinate de chlorhy dro xy d'aluminium est "alcloxa" : Oxyde d'aluminium (28,0 ± 3)%, allantoïne (40,0 ± 3)%, chlore (9,5 ± 1,5)%, azote (14,2 ± 1,5)%.
Parallèlement, la composition de l'allantoïne chloroaluminique modifiée est la suivante : Oxyde d'aluminium (45,61 ± 2,0)%, allantoïne (1,25 ± 0,3)%, chlore (15,60 ± 1,5). Le pH de la solution 10% d'allantoïne chlorhydrique d'aluminium est d'environ 4,3.
D'après la littérature, les principales méthodes de synthèse de l'allantoïne sont les suivantes :
1. Réaction de l'acide urique avec le permanganate de potassium
L'acide urique et le permanganate de potassium sont oxydés en milieu alcalin et les produits sont décarboxylés avec de l'acide acétique. Les oxydants peuvent également être le dioxyde de plomb, le ferricyanure de potassium, l'oxygène, l'ozone, le dioxyde de manganèse, le peroxyde d'hydrogène, etc. Le processus de réaction est le suivant :
Tout d'abord, la réaction d'oxydation. L'acide urique et le permanganate de potassium réagissent.
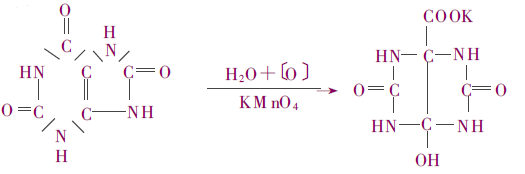
La réaction de décarboxylation et d'ouverture du cycle permet ensuite d'obtenir le produit final.
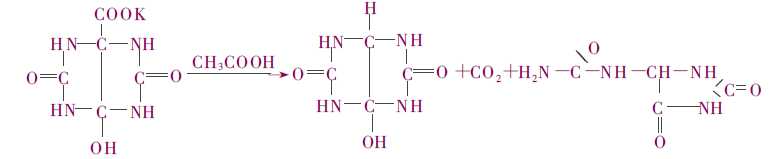
Il s'agit du processus le plus précoce, qui est limité à la production de petits lots en raison de la pénurie de matières premières, du prix élevé, du grand volume d'équipement et du coût élevé.
2. Oxydation électrolytique de l'urate de lithium
L'allantoïne a été synthétisée par condensation de l'acide glyoxylique et de l'urée sous l'effet de l'électricité.
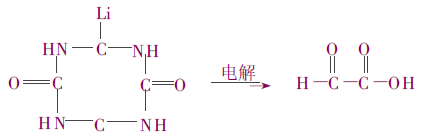
Bien que le rendement de cette méthode soit légèrement supérieur à celui de la méthode d'oxydation de l'acide urique, elle présente également les problèmes susmentionnés et a moins d'applications industrielles.
3. Oxydation électrolytique de l'acide oxalique
Il s'agit d'un nouveau procédé mis au point ces dernières années, et cette ligne de production a été mise en place en Chine. Les matières premières sont faciles à obtenir, mais la consommation d'énergie est importante. D'après la littérature, le processus n'est pas mûr et doit être amélioré.
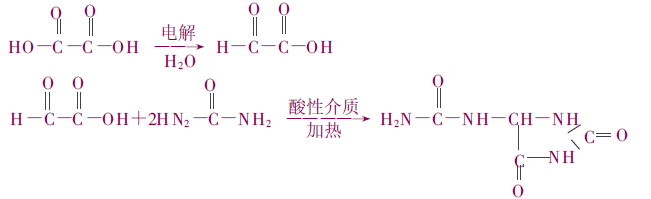
4. Oxydation du glyoxal
Comme l'acide glyoxylique peut être préparé par oxydation partielle du glyoxal et que les conditions du processus sont douces, cette voie de synthèse est souvent utilisée dans l'industrie. Toutefois, cette méthode utilise de l'acide nitrique pour l'oxydation, ce qui entraîne une grave pollution de l'environnement.
Tout d'abord, oxydation partielle du glyoxal pour obtenir l'acide glyoxylique.
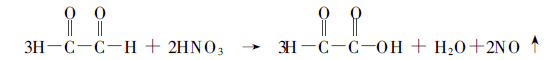
Le rendement de cette méthode d'obtention de l'acide glyoxylique est donc d'environ 83%.
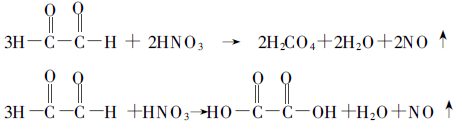
Ensuite, synthèse de l'allantoïne par condensation de l'acide glyoxylique et de l'urée dans des conditions de chauffage et d'acidité.
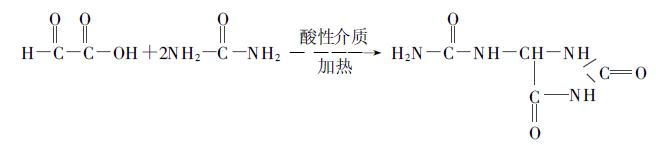
La conversion de l'acide glyoxylique par cette voie est de 52% ~ 58%. Selon toutes les réactions, comptées par le glyoxal, le rendement en allantoïne est de 38% - 40% de la valeur théorique.
5. Réaction de l'urée avec l'acide dichloracétique
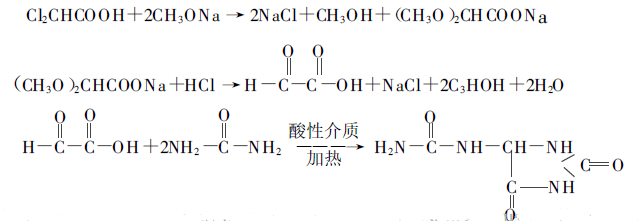
Il est préparé en chauffant 2 mol d'urée et 1 mol d'acide dichloracétique. Le processus de réaction est le suivant :
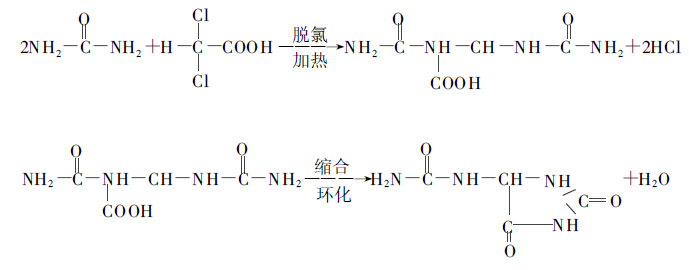
Dans les années 1930, un brevet américain a signalé que l'allantoïne pouvait être produite dans de l'éthylène glycol à 120 ℃ pendant 4 heures, mais le rendement était faible. Le rendement total de l'acide allantoïne-p-dichloroacétique peut atteindre 30,3%. Certains chercheurs chinois ont étudié le processus et ont obtenu un rendement total d'allantoïne supérieur à 40%. Le processus complet est le suivant.
À l'heure actuelle, d'autres voies de développement technologique et de recherche sont également très actives, essayant de réussir à moindre coût, comme la méthode de l'acétylène, le dioxyde de carbone, le monoxyde de carbone et d'autres méthodes de récupération des gaz résiduaires à haute teneur. Toutefois, aucun rapport n'a encore été mis en production. En tant que produit industriel important, l'allantoïne a besoin de plus de recherche synthétique pour être soutenue.
Où acheter Allantoin?
Longchang Chemical est spécialisé dans la production et la fourniture d'Allantoïne CAS 97-59-6. Nous vous contacterons généralement dans les 24 heures. Vous pouvez également m'envoyer un e-mail à l'adresse info@longchangchemical.com pendant les heures de travail ( 8:30 am to 6:00 pm UTC+8 Mon.~Sat. ) ou utiliser le chat en direct du site web pour obtenir une réponse rapide.
Cet article a été rédigé par Longchang Chemical R&D Department. Si vous souhaitez le copier ou le réimprimer, veuillez en indiquer la source..
A practical selection checklist for wetting, leveling, and defoaming additives
Additive selection is usually most effective when the team defines the defect first and then screens compatibility, dosage range, and process stage. That is often much more reliable than choosing only by chemistry family or by a single dramatic lab result.
- Start from the defect, not the additive name: wetting loss, crater, microfoam, and instability often need different solutions even inside the same formula.
- Check compatibility at the intended dosage: the strongest additive can still be the wrong commercial choice if it narrows the process window too much.
- Review the stage of use: some products are most useful during grind, while others matter more during let-down, filling, or final application.
- Balance cure or film quality with defect control: the right additive fixes the problem without sacrificing adhesion, gloss, or appearance.
Recommended product references
- CHLUMIAF 094: A balanced defoamer reference for waterborne coatings and many general foam-control screens.
- CHLUMIAF 3062: Useful when printing-ink and UV-ink compatibility matter in the defoaming screen.
- CHLUMIAF 3037: A stronger process-defoaming option when persistent foam survives harsher conditions.
- CHLUMIWE 3280: A strong wetting-agent reference for inks, coatings, and difficult substrate wetting.
FAQ for buyers and formulators
Why does an additive that looks powerful in a beaker sometimes fail in production?
Because shear, temperature, substrate, and the full formula can all change the way the additive performs under real process conditions.
Should the most aggressive additive always be preferred?
Not usually. The best additive is the one that solves the real defect while preserving the broadest safe operating window.
